Columbia University Irving Medical Center
Mit Hilfe von Echtzeit-Bildern aus dem Inneren der Lunge haben Forscher des Vagelos College of Physicians and Surgeons herausgefunden, wie ein gefährlicher Staphylokokken-Stamm die anfänglichen Abwehrmechanismen der Lunge umgeht und innerhalb von 10 Minuten einen Prozess in Gang setzt, der die Lunge schwer schädigt.
Staphylococcus aureus, insbesondere der epidemische Stamm USA300, ist eine der Hauptursachen für Lungenentzündungen bei Krankenhauspatienten und verursacht häufig Lungenentzündungen bei zuvor gesunden Menschen mit Grippe.
Um herauszufinden, wie sich USA300 zuerst in der Lunge etabliert, injizierte ein Team von Forschern der Abteilungen Medizin und Pädiatrie – Jaime Hook, MD, Naeem Islam, PhD, Dane Parker, PhD, Alice Prince, MD, Sunita Bhattacharya, MD, und Jahar Bhattacharya, MD, DPhil – fluoreszierende USA300-Bakterien in eine lebende Mauslunge. Anschließend beobachteten sie, was mit den Bakterien und den Lungenbläschen geschah.
Eine Live-Darstellung der intakten Lungenbläschen ist nicht einfach. Das Bhattacharya-Labor hat einen Ansatz entwickelt, bei dem fluoreszierende Farbstoffe durch feine Glasnadeln in die Lungenbläschen injiziert werden können, wodurch die Lungenbläschen durch konfokale Mikroskopie optisch anschaulich werden.
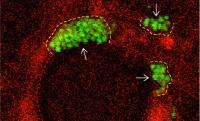
Die Bilder zeigten, dass sich die USA300-Bakterien innerhalb von 10 Minuten nach dem Eindringen in die Lunge in den Luftsäcken der Lunge zusammenballen. In diesen Aggregaten konnten die Bakterien einem Abwehrmechanismus der Lunge entgehen: einer dünnen Schicht fließender Flüssigkeit, die normalerweise Bakterien aus den Lungenbläschen herausspült.
MRSA-Aggregate in den Winkeln der Lungenbläschen
Die USA300-Aggregate waren auch von dem Antibiotikum Vancomycin unbeeinflusst, das USA300-Bakterien in vitro abtöten kann, aber bei Lungenentzündungspatienten eher unwirksam ist.
Mit ihrem bildgebenden System sahen die Forscher, dass Vancomycin die USA300 in der Lunge nicht bekämpft, weil es die bakteriellen Aggregate nicht durchdringen kann.
Vancomycin wirkte nur dann gegen die USA300-Bakterien in der Lunge, wenn das PhnD-Gen des Bakteriums inaktiviert wurde oder wenn ein Antikörper, der PhnD blockiert, in die Lunge eingebracht wurde. In-vitro-Studien haben gezeigt, dass PhnD dazu beiträgt, Bakterien zu einem Biofilm zu verbinden; die neue Studie ist die erste, die zeigt, dass PhnD auch in intakten Lungenbläschen auf diese Weise funktioniert.
Auch beim Menschen ist PhnD wahrscheinlich entscheidend für die Entstehung von USA300-Infektionen: Die Forscher fanden heraus, dass die Bakterien auch in der menschlichen Lunge in Winkeln aggregieren.
„Die Studie zeigt, dass biofilmartige Aggregate bei der Etablierung von USA300-Infektionen in der Lunge wichtig sind“, sagt Sunita Bhattacharya, „und dass die gezielte Bekämpfung von PhnD oder die Suche nach anderen Möglichkeiten, bakterielle Aggregate aufzulösen, helfen könnte, USA300-induzierte Lungenverletzungen zu verhindern.