Columbia University Irving Medical Center
En utilisant l’imagerie en temps réel de l’intérieur du poumon, les chercheurs du Vagelos College of Physicians and Surgeons ont appris comment une souche dangereuse de Staph échappe aux mécanismes de défense initiaux du poumon et, en 10 minutes, entame un processus qui endommage gravement le poumon.
Staphylococcus aureus, en particulier la souche épidémique USA300, est une cause majeure de pneumonie chez les patients hospitalisés et provoque souvent une pneumonie chez des personnes auparavant en bonne santé et atteintes de la grippe.
Pour savoir comment l’USA300 s’établit d’abord dans le poumon, une équipe de chercheurs des départements de médecine et de pédiatrie-Jaime Hook, MD, Naeem Islam, PhD, Dane Parker, PhD, Alice Prince, MD, Sunita Bhattacharya, MD, et Jahar Bhattacharya, MD, DPhil-a injecté des bactéries USA300 fluorescentes dans un poumon de souris vivant. Ils ont ensuite observé ce qui est arrivé aux bactéries et aux sacs aériens.
L’imagerie en direct des sacs aériens intacts du poumon n’est pas facile. Le laboratoire de Bhattacharya a mis au point une approche dans laquelle des colorants fluorescents peuvent être injectés dans les sacs aériens par de fines aiguilles de verre, rendant les sacs aériens optiquement vivants par microscopie confocale.
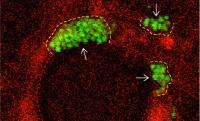
Les images ont montré que dans les 10 minutes suivant l’entrée dans le poumon, les bactéries USA300 s’agglutinent dans les recoins des sacs aériens du poumon. Dans ces agrégats, les bactéries ont pu échapper à l’un des mécanismes de défense du poumon : une fine couche de liquide fluide qui balaie normalement les bactéries hors des sacs aériens.
Les agrégats de SARM dans les recoins des sacs aériens du poumon
Les agrégats d’USA300 n’étaient pas non plus affectés par l’antibiotique vancomycine, qui peut tuer les bactéries USA300 in vitro mais a tendance à être inefficace chez les patients atteints de pneumonie.
Avec leur système d’imagerie, les chercheurs ont vu que la vancomycine ne parvient pas à combattre la bactérie USA300 dans le poumon parce qu’elle ne peut pas pénétrer dans les agrégats bactériens.
La vancomycine n’a fonctionné contre la bactérie USA300 dans le poumon que lorsque le gène PhnD de la bactérie avait été inactivé ou lorsqu’un anticorps qui bloquait PhnD était introduit dans le poumon. Des études in vitro ont montré que PhnD aide à relier les bactéries entre elles pour former un biofilm ; la nouvelle étude est la première à montrer que PhnD fonctionne également de cette manière à l’intérieur des sacs aériens intacts du poumon.
Chez les humains, PhnD est également susceptible d’être critique dans l’établissement des infections à USA300 : les chercheurs ont constaté que les bactéries s’agrégeaient également dans des recoins à l’intérieur des poumons humains.
« L’étude montre que les agrégats de type biofilm sont importants dans l’établissement des infections à USA300 dans le poumon », explique Sunita Bhattacharya, « et que le fait de cibler PhnD ou de trouver d’autres moyens de briser les agrégats bactériens pourrait aider à prévenir les lésions pulmonaires induites par USA300 ».