Proteínas de Ciclina Herramientas de Investigación – Creative BioMart
La Ciclina es una familia de proteínas que regulan el ciclo celular mediante quinasas dependientes de ciclina. Son proteínas que suben y bajan en tándem con el ciclo celular de las células eucariotas, aisladas por primera vez de embriones de erizos de mar, son proteínas de masa molecular relativa 50.000. Una gran familia, que incluye: proteínas periódicas A, B, D, E, G y H. Se unen a proteínas quinasas clave (quinasas dependientes de ciclina, CDKs) y regulan su actividad enzimática, ayudando a avanzar y coordinar la progresión del ciclo celular.
Estructura
La estructura de las ciclinas se muestra en la figura siguiente, y la estructura primaria no suele ser la misma. La ciclina contiene dos dominios similares, el primero en el N-terminal y el segundo en el C-terminal. La estructura terciaria de dos dominios estrechos de cinco hélices alfa. El primero es un casete de ciclina conservado en el que los ciclones convergen fuera de la célula. Por ejemplo, la región aminoterminal de las ciclinas S y M comprende un motivo corto de caja de seguridad que se dirige a la proteólisis en la mitosis.
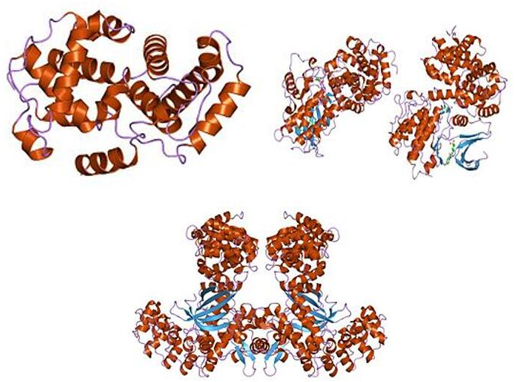 Figura 1. Ciclina, dominio N-terminal, Ciclina, dominio C-terminal y Ciclina K, C terminal.
Figura 1. Ciclina, dominio N-terminal, Ciclina, dominio C-terminal y Ciclina K, C terminal.
Proteínas relacionadas con las Proteínas de Ciclina
La fase G2/M está regulada principalmente por la quinasa CDK1, que está compuesta por la quinasa CDK1, el MPF, o la proteína P34cdc2 y la ciclina B. La proteína CDK1 por sí misma no tiene actividad de proteína quinasa. Cuando el contenido de ciclina A/B se acumula hasta un cierto valor, las dos se combinan en un complejo, la CDK1 que se une a la ciclina fosforila Thr14 y Tyr15 por Wee1, y fosforila Thr161 por la quinasa activada por la CDK. En la fase M, la actividad de Wee1 disminuye, y cdc25 desfosforila Thr14 y Tyr15 de CDK1, y su actividad quinasa se expresa. En la fase G2/M, la ciclina A y la ciclina B se unen a CDK1, y CDK1 fosforila la proteína sustrato. Por ejemplo, la fosforilación de la histona H1 conduce a la condensación del cromosoma, y la fosforilación de la laminina provoca la desintegración de la membrana nuclear. En la fase M, cuando la actividad del MPF alcanza su máximo, se activa el factor promotor tardío APC, y la ubiquitina se liga a la ciclina A y a la ciclina B. Mediante la poliubiquitinación, son degradadas por el proteasoma para completar un ciclo celular.
CDK (cinasa dependiente de ciclina)
Las proteínas cinasas dependientes de ciclina son un grupo de proteínas cinasas de serina/treonina. Las CDK impulsan el ciclo celular mediante la acción química de las proteínas de serina/treonina. La sinergia con la ciclina ciclina es importante en la regulación del ciclo celular. factor. La CDK puede formar un heterodímero con la ciclina, en el que la CDK es una subunidad catalítica, la ciclina es una subunidad reguladora, y diferentes complejos ciclina-CDK catalizan la fosforilación de diferentes sustratos por la actividad de la CDK, logrando así diferentes tiempos del ciclo celular. La promoción y la transformación de la fase. La actividad de la CDK depende de la expresión secuencial de su subunidad reguladora positiva ciclina y de su concentración de subunidad reguladora negativa CKI (inhibidor de la quinasa dependiente de ciclina, inhibidor de la CDK). Al mismo tiempo, la actividad de la CDK también está regulada por la fosforilación y la desfosforilación, así como por oncogenes y genes supresores de tumores.
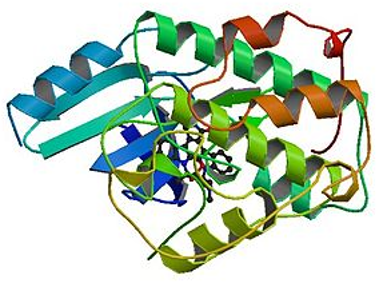 Figura 2. Estructura de la proteína CDK.
Figura 2. Estructura de la proteína CDK.
Significado
Los científicos han descubierto que varios tipos de factores reguladores desempeñan un papel importante en el ciclo celular. Un tipo es un factor de crecimiento celular que regula la división y proliferación celular. Por ejemplo, el segundo tipo de regulador del ciclo celular, también conocido como regulador endógeno, es una proteína autosintetizada en las células. Se ha abierto la antesala del mecanismo de regulación del ciclo celular. Los científicos están estudiando la relación entre el ciclo celular y los oncogenes, los genes supresores de tumores, los factores de crecimiento y la proliferación y diferenciación celular desde diferentes perspectivas. Creo que a través del trabajo duro, podemos finalmente encontrar la magia para controlar el ciclo celular. «interruptor». En el tratamiento del cáncer, también podemos utilizar el principio del ciclo celular para prescribir el medicamento adecuado. Si las células G0 no son sensibles a la quimioterapia, a menudo se convierten en la causa principal de la recurrencia del cáncer en el futuro. Por lo tanto, se puede intentar inducir a las células cancerosas en fase G0 para que entren en el ciclo proliferativo y luego las maten. Esta es una cuestión de importancia teórica y práctica en la exploración.