Cyclin Proteins Research Tools – Creative BioMart
Cyclin to rodzina białek, które regulują cykl komórkowy poprzez kinazy zależne od cykliny. Białka, które wznoszą się i opadają w tandemie z cyklem komórkowym komórek eukariotycznych, po raz pierwszy wyizolowane z embrionów jeżowca, mają względną masę cząsteczkową 50 000 białek. Jest to duża rodzina, obejmująca: białka okresowe A, B, D, E, G i H. Wiążą się one z kluczowymi kinazami białkowymi (kinazami zależnymi od cykliny, CDK) i regulują ich aktywność enzymatyczną, pomagając w przyspieszeniu i koordynacji progresji cyklu komórkowego.
Struktura
Strukturę cyklin przedstawiono na poniższym rysunku. Cyklina zawiera dwie podobne domeny, pierwszą na N-końcu i drugą na C-końcu. Struktura trzeciorzędowa dwóch ciasnych domen składa się z pięciu heliksów alfa. Pierwszą z nich jest konserwowana kaseta cykliny, w której cyklony zbiegają się na zewnątrz komórki. Na przykład region amino-końcowy cyklin S i M obejmuje krótki motyw lock box, który jest celem proteolizy w mitozie.
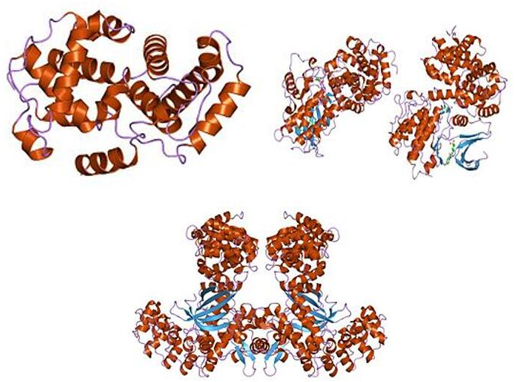 Rysunek 1. Cyclin, N-terminal domain, Cyclin, C-terminal domain and K cyclin, C terminal.
Rysunek 1. Cyclin, N-terminal domain, Cyclin, C-terminal domain and K cyclin, C terminal.
Białka związane z Cyclin Proteins
Faza G2/M jest regulowana głównie przez kinazę CDK1, która składa się z kinazy CDK1, MPF, lub białka P34cdc2 i cykliny B. Samo białko CDK1 nie posiada aktywności kinazy białkowej. Gdy zawartość cykliny A/B skumuluje się do pewnej wartości, obie łączą się w kompleks, CDK1 wiążąc się z cykliną fosforyluje Thr14 i Tyr15 przez Wee1, a fosforyluje Thr161 przez kinazę aktywowaną przez CDK. W fazie M aktywność Wee1 jest obniżona, a cdc25 fosforyluje Thr14 i Tyr15 CDK1, a jej aktywność kinazowa jest wyrażona. W fazie G2/M, cyklina A i cyklina B wiążą się z CDK1, a CDK1 fosforyluje białko substratowe. Na przykład, fosforylacja histonu H1 prowadzi do kondensacji chromosomów, a fosforylacja lamininy powoduje rozpad błony jądrowej. W fazie M, kiedy aktywność MPF osiąga maksimum, aktywowany jest czynnik późnego promowania APC, a ubikwityna jest wiązana do cyklin A i B. Poprzez polikwitynację są one degradowane przez proteasom, aby zakończyć cykl komórkowy.
CDK (Cyclin-dependent kinase)
Kinazy białkowe zależne od cyklin to grupa serynowo-treoninowych kinaz białkowych. CDK napędzają cykl komórkowy poprzez chemiczne działanie białek serynowych/treoninowych. Synergistycznie z cykliną cyclin jest ważny w regulacji cyklu komórkowego. factor. CDK może tworzyć heterodimer z cykliną, w którym CDK jest podjednostką katalityczną, cyklina jest podjednostką regulatorową, a różne kompleksy cyklina-CDK katalizują fosforylację różnych substratów przez aktywność CDK, osiągając w ten sposób różne czasy cyklu komórkowego. Promocja i transformacja fazy. Aktywność CDK zależy od sekwencyjnej ekspresji jej pozytywnej podjednostki regulatorowej cykliny i stężenia jej negatywnej podjednostki regulatorowej CKI (inhibitora kinazy zależnej od cykliny, inhibitora CDK). Jednocześnie aktywność CDK jest również regulowana przez fosforylację i deposforylację, a także onkogeny i geny supresorowe nowotworów.
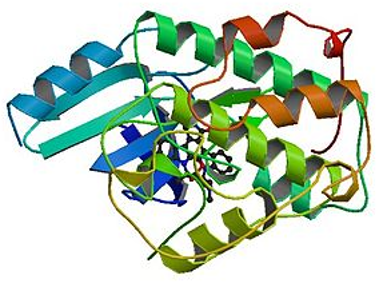 Rysunek 2. Struktura białka CDK.
Rysunek 2. Struktura białka CDK.
Znaczenie
Naukowcy odkryli, że kilka typów czynników regulacyjnych odgrywa ważną rolę w cyklu komórkowym. Jednym z nich jest czynnik wzrostu komórek, który reguluje podziały i proliferację komórek. Na przykład, drugi typ regulatora cyklu komórkowego, znany również jako regulator endogenny, jest białkiem samoistnie syntetyzowanym w komórkach. Preludium do mechanizmu regulacji cyklu komórkowego zostało otwarte. Naukowcy z różnych perspektyw badają związek między cyklem komórkowym a onkogenami, genami supresorowymi nowotworów, czynnikami wzrostu oraz proliferacją i różnicowaniem komórek. Wierzę, że dzięki ciężkiej pracy, możemy w końcu znaleźć magię, aby kontrolować cykl komórkowy. „przełącznik”. W leczeniu raka, możemy również wykorzystać zasadę cyklu komórkowego do przepisania odpowiedniego leku. Jeśli komórki G0 nie są wrażliwe na chemioterapię, często stają się pierwotną przyczyną nawrotów raka w przyszłości. Dlatego można próbować indukować komórki nowotworowe w fazie G0 do wejścia w cykl proliferacyjny, a następnie zabić. Jest to zagadnienie o znaczeniu teoretycznym i praktycznym w badaniach.