Punteros de ECG: Marcapasos… y cuando funcionan mal
Autor: David Bussé, MD, MBA (Médico residente de EM, UTSW / Parkland Memorial Hospital) // Editado por: Jamie Santistevan, MD (@jamie_rae_EMdoc – Médico de EM, Hospital Presbiteriano, Albuquerque, NM); Manpreet Singh, MD (@MPrizzleER – Profesor Asistente de Medicina de Emergencia / Departamento de Medicina de Emergencia – Centro Médico Harbor-UCLA); y Brit Long, MD (@long_brit – EM Attending Physician, San Antonio, TX)
Bienvenidos a esta edición de ECG Pointers, una serie de emDOCs diseñada para darle consejos de alto rendimiento sobre los ECGs para mantener sus habilidades de interpretación afiladas. Para profundizar en los ECGs, incluiremos enlaces a otros grandes ECG FOAMed!
El caso:
Un hombre de 76 años con HTA, DM, EAC y bloqueo cardíaco de 3er grado tras la colocación de un marcapasos hace 8 años se presenta en su servicio de urgencias con disnea de esfuerzo y un episodio de síncope hoy temprano. Sus constantes vitales de triaje son T 37,2C, FC 38, PA 118/78, RR 18, y O2 Sat 96% en aire ambiente. El paciente que tiene delante tiene buen aspecto y responde adecuadamente a las preguntas. Es capaz de afirmar que, por cuestiones de seguro, no ha podido concertar una cita con un cardiólogo en los últimos 3 años.
Su ECG inicial revela lo siguiente:
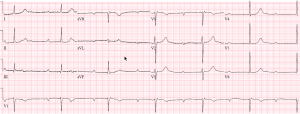
Función del marcapasos

Los marcapasos están formados por múltiples componentes:
- El generador de impulsos contiene la batería. Se implanta en los tejidos blandos o en los músculos de la pared torácica anterior. La mayoría de los marcapasos tienen una duración de la batería de entre 5 y 10 años. La duración de la batería depende de la frecuencia con la que el marcapasos detecta y marca el ritmo, lo que dificulta la predicción exacta de su duración. La sustitución oportuna requiere un seguimiento adecuado.
- Los cables del marcapasos conectan el generador de impulsos al miocardio. Los cables se colocan en el ventrículo derecho para los marcapasos monocamerales. Los marcapasos bicamerales tienen cables en la aurícula y el ventrículo derechos. Por último, los marcapasos biventriculares (de resincronización) colocan cables en la aurícula derecha, el ventrículo derecho y el seno coronario (que estimula el ventrículo izquierdo). La fractura de los cables o la rotura del revestimiento aislante pueden provocar una funcionalidad inadecuada del marcapasos/sensor.
- La estimulación se produce cuando se aplica una diferencia de potencial (voltaje) entre dos electrodos. El umbral de estimulación es la cantidad mínima de energía necesaria para despolarizar el miocardio, descrita por la amplitud (voltios) y la duración. Estas características son programables y afectan a la longevidad de la batería .
Los marcapasos se describen completamente mediante un código de 5 posiciones, en el que las 3 primeras definen la función del dispositivo . Se pueden recordar mediante la nemotecnia PaSeR1: función de estimulación, posición de detección y respuesta a la detección.
La configuración más común para los dispositivos de doble cámara es DDD, en la que el marcapasos estimula y detecta tanto la aurícula como el ventrículo. Si se detecta un latido nativo, el marcapasos se inhibe. Si no se detecta ningún latido nativo después de un intervalo de tiempo determinado, el marcapasos emite un latido desencadenado.
Este es un paciente con un marcapasos DDD que funciona normalmente:
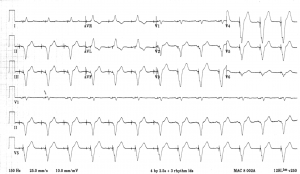
Fallo del marcapasos
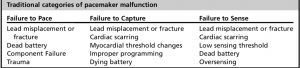
El fallo del marcapasos se ha dividido tradicionalmente en 3 categorías:
- El fallo del marcapasos sugiere que el generador de pulsos no está proporcionando una salida de voltaje suficiente para despolarizar el miocardio. El ECG no muestra ni picos de marcapasos ni complejos QRS inducidos por el marcapasos, sino el ritmo nativo del paciente.
- El fallo de captura se produce cuando se da un pulso de marcapasos, pero el impulso es incapaz de despolarizar el tejido miocárdico no refractario. Los picos del marcapasos se ven en un ECG, pero no hay respuesta cardíaca. Una vez más, se observa el ritmo nativo del paciente en el ECG. La fibrosis de la respuesta inflamatoria local semanas después de la implantación (disminución de la incidencia debido a los cables liberadores de esteroides ) además de la fractura/desconexión del cable, el síndrome de twiddler y la perforación cardíaca pueden ser los culpables .
- El fallo de detección incluye tanto el sobresensado como el infrasensado. Con el sobresensado, el marcapasos interpreta erróneamente otras señales (picos de ondas T, interferencias electromagnéticas, actividad del músculo esquelético) como complejos QRS, inhibiendo la respuesta y no iniciando la estimulación . Con la infrasensibilidad, el marcapasos es incapaz de interpretar correctamente la actividad cardíaca nativa debido a los cambios en las señales intracardíacas (isquemia miocárdica, nuevos bloqueos de rama del haz, PVC). La sensibilidad se puede reprogramar para mejorar estos problemas .
- Esta categorización histórica tiene poco valor en el contexto agudo, ya que sus causas tienden a superponerse en gran medida, y todas ellas se manejan de forma similar.
- Sospeche de una disfunción del marcapasos con quejas de aturdimiento, fatiga, palpitaciones, hipo, confusión, disnea, espasmos musculares y síncope.
- La historia debe indicar si el paciente tiene algún problema subyacente que provoque un mal funcionamiento del marcapasos. Estos incluyen SCA, traumatismos, cambios de medicación o reprogramación reciente del dispositivo .
- Los pacientes reciben tarjetas con el tipo de dispositivo, el modelo, el fabricante y la fecha de implantación del dispositivo.
- Pide a los pacientes que proporcionen su tarjeta de marcapasos.
- El examen físico debe comenzar con una revisión de los signos vitales, el estado mental y el estado cardiopulmonar. Observe los signos de infección, migración o traumatismo en el lugar del implante. Busque también JVD, ondas de cañón A, contracciones del músculo pectoral y nuevos soplos/rubores cardíacos.
- Obtenga un ECG para determinar si existe una bradicardia inestable. Compárelo con ECGs anteriores, fijándose especialmente en los cambios de eje .
- El ECG de un paciente con ritmo ventricular único mostrará picos de marcapasos ventricular y un BRI con desviación del eje izquierdo debido a la colocación del electrodo en el VD .
- Los marcapasos biventriculares que capturan la pared libre del VI demuestran una onda R dominante en V1 y un complejo QS en la derivación I, lo que indica un frente de onda que se propaga fuera del VI6.
- Los segmentos ST y las ondas T deben ser discordantes con el QRS.
-
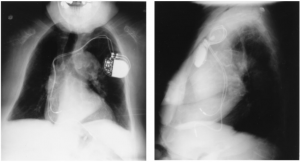
Obtenga radiografías de tórax PA y laterales para comprobar si hay desprendimiento de cables, fractura o neumotórax. En caso de que un paciente no pueda presentar la tarjeta del marcapasos, se puede utilizar una radiografía de tórax sobrepenetrada para determinar el fabricante del dispositivo mediante la identificación del símbolo de la empresa .
- Obtenga mediciones séricas de electrolitos y de cualquier fármaco cardiotóxico, además de biomarcadores cardíacos en el entorno adecuado. Los desórdenes metabólicos, incluidos el hipotiroidismo, la acidosis y la hipopotasemia, pueden alterar el potencial umbral necesario para la estimulación .
- El manejo está dictado por los síntomas del paciente y el estado hemodinámico. Los parches de estimulación transcutánea deben colocarse en el paciente en una configuración anterior-posterior siempre que se sospeche un mal funcionamiento . Aplicar los protocolos estándar de ACLS en caso de que el paciente esté bradicárdico con síntomas de hipoperfusión.
- Cuando esté hemodinámicamente estable, interrogar al marcapasos. El interrogatorio proporciona información sobre la duración de la batería, los umbrales de detección y estimulación (infradetección/sobredetección), la integridad del sistema de cables (fractura de cables) y los registros del ritmo cardíaco . El interrogatorio puede indicar el buen funcionamiento o la presencia de arritmias que ayudan a estratificar el riesgo del paciente.
- El interrogatorio implica la comunicación por radiofrecuencia con el marcapasos mediante la colocación de una varita sobre el dispositivo. La varita está unida a un programador que realiza el interrogatorio, y es específico de cada compañía de dispositivos.
Este es un ejemplo de un paciente con bradicardia a pesar de la colocación del marcapasos:
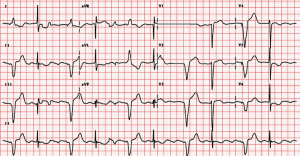
Disritmias/Síndromes inducidos por el marcapasos:
- Aplicar los criterios de Sgarbossa a los pacientes con marcapasos ante la sospecha de SCA.
- La taquicardia mediada por marcapasos (TPM) es una taquicardia de bucle reentrante exclusiva de los marcapasos bicamerales . Se envía una PVC a las aurículas de forma retrógrada. Esta despolarización ventricular estimula la detección auricular, desencadenando otra despolarización ventricular; se crea un bucle que establece la disritmia en el límite superior de la frecuencia del marcapasos. Un imán clínico o cualquier terapia que aumente el periodo refractario en el nodo AV (adenosina, BCC, BB) terminará con la arritmia .
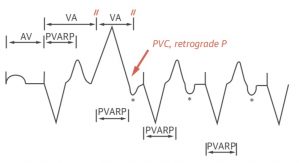
Taquicardia mediada por marcapasos: El primer latido ilustra la estimulación secuencial AV, seguida por un latido de PVC. El PVC inicia un nuevo intervalo VA. Cualquier evento de desacoplamiento AV (más frecuentemente PVCs) puede conducirse de forma retrógrada a la aurícula. Se detecta un evento auricular si cae fuera del periodo refractario auricular posventricular (PVARP). El intervalo VA expira y se desencadena un nuevo intervalo AV. La estimulación ventricular se produce al final del intervalo AV estableciendo una serie tortuosa de eventos denominada taquicardia mediada por marcapasos.
- El «comportamiento de frecuencia superior» puede inducir un bloqueo 2:1 . En el modo de estimulación bicameral, el dispositivo estimula de forma 1:1 (A:V) hasta alcanzar la frecuencia ventricular superior programada. A medida que la frecuencia auricular aumenta, la estimulación ventricular no puede violar el límite superior de la frecuencia, lo que resulta en intervalos AV progresivamente más largos. A medida que el intervalo AV se alarga, puede desarrollarse un bloqueo abrupto 2:1 con una ralentización repentina de la frecuencia ventricular (la frecuencia ventricular se convierte en la mitad de la frecuencia máxima de rastreo), induciendo síntomas .
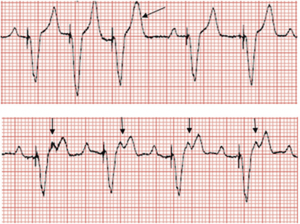
Comportamiento de la frecuencia superior en un marcapasos de doble cámara: Con un aumento de la frecuencia sinusal por encima de 130 lpm, algunas de las ondas P caen en el periodo PVARP (flechas) y no son rastreadas. Se observa una prolongación progresiva del PR antes de los latidos bloqueados (Wenckebach del marcapasos). Cuando la frecuencia sinusal alcanza el TARP (intervalo AV + PVARP), todas las demás ondas P caen en el PVARP y no son rastreadas, lo que da lugar a una frecuencia ventricular efectiva de 75 lpm, y a una caída abrupta de la frecuencia cardíaca (frecuencia de bloqueo 2:1 en este paciente). No se trata de ondas p retrógradas.
- Un «marcapasos desbocado» implica una disfunción del generador del marcapasos . La frecuencia del marcapasos es superior al límite superior programado (hasta 400 lpm). Se utilizan imanes clínicos para abortar la arritmia. El último recurso es desconectar los cables del generador de impulsos (cortando el bolsillo).
- El síndrome de Twiddler se produce cuando los pacientes alteran/desconectan los cables manipulando el generador . Una RX mostrará la torsión de los cables sobre el generador. La corrección quirúrgica es necesaria.
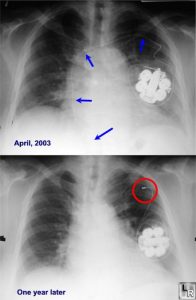
Consulta este post en Learning Radiology: http://learningradiology.com/archives05/COW%20141-Twiddlers%20Syndrome/twiddlerscorrect.htm
- El síndrome del marcapasos describe los síntomas anormales del paciente (disnea, mareos, dolor torácico, palpitaciones) tras descartar todas las demás causas de mal funcionamiento del marcapasos. Común a los marcapasos monocamerales, se cree que se debe a una relación de despolarización anormal entre las aurículas y los ventrículos, o disincronía AV . Se corrige optimizando los modos de estimulación/programación.
- El uso de la RMN en pacientes con marcapasos está contraindicado dado el riesgo de desencadenar una estimulación de alta frecuencia . Los marcapasos condicionales a la RMC están diseñados específicamente para ser seguros en un entorno de RM, pero estos representan la gran minoría de dispositivos. Los dispositivos condicionados por la RMC tienen un material ferromagnético mínimo, un filtrado alterado y conductores de plomo rediseñados para minimizar la inducción de corriente y el calentamiento del tejido .
Consideraciones adicionales:
- Los pacientes pueden acudir a urgencias poco después de la colocación del marcapasos con dolor e inflamación en el lugar del bolsillo.
- La hemorragia en el bolsillo es una complicación común, y puede disecar planos fasciales . Los hematomas grandes requieren una evacuación quirúrgica. ¡No se debe aspirar!
- El eritema, el edema, la fluctuación y la dehiscencia del lugar de la incisión son indicativos de infección. La mayoría de las infecciones son causadas por S. aures y S. epidermidis, por lo que se debe iniciar una cobertura empírica con vancomicina en el servicio de urgencias .
- Las infecciones que surgen más tarde suelen afectar a los cables del marcapasos . Sospechar bacteriemia, vegetaciones de los cables y émbolos pulmonares sépticos. Confirmar el diagnóstico con hemocultivos y ETE. La vancomicina es de nuevo el antibiótico de elección, ya que las bacterias causantes suelen ser grampositivas. La terapia definitiva incluye la extracción quirúrgica del plomo .
- La colocación de un marcapasos también puede provocar derrames pericárdicos, neumotórax y hemotórax . Espere estas presentaciones alrededor de 48 horas después del procedimiento con quejas de disnea, dolor torácico y enfisema subcutáneo.
- La colocación del plomo a través de la válvula tricúspide puede provocar una disfunción valvular .
- Los marcapasos también pueden migrar a planos fasciales más superficiales debido a traumatismos, hematomas o isquemia tisular local. Dicha migración puede causar la erosión de la pared del bolsillo, lo que hace necesario el desbridamiento quirúrgico y la reubicación .
- Dado que los cables entran en la VCS, las TVP pueden desarrollarse poco después de la inserción o años después de la implantación. Se ha notificado el síndrome de la VCS secundario a la trombosis venosa .
- La TEV también puede aumentar el riesgo de hipertensión pulmonar y de accidente cerebrovascular en los casos de foramen oval permeable .
- El tratamiento es la anticoagulación precoz, pero no se suele retirar el cable, ya que hacerlo puede provocar la extensión del trombo .
- El desprendimiento del electrodo y la migración desde la interfaz miocárdica son complicaciones comunes en los primeros 1-2 días tras la implantación . La adherencia fibrinosa del electrodo tras la implantación tiende a evitar el desprendimiento tardío. No obstante, el riesgo persiste dado el estrés mecánico repetitivo de cada ciclo cardíaco y el movimiento de la cintura escapular.
- Busque cables desprendidos en la RX en el seno coronario, el VI, la VCI, la VCS, la arteria pulmonar o en la aurícula fuera del apéndice.
- El desprendimiento de cables también puede causar trombosis de la vena pulmonar, perforación del miocardio y disritmias .
- La mala posición del cable puede provocar la estimulación del nervio frénico con la consiguiente excitación diafragmática e hipo intratable . Se ha informado de una mayor incidencia de estimulación diafragmática con marcapasos de resincronización .
- Muchas de estas preocupaciones pueden mitigarse en un futuro próximo con la llegada de los marcapasos sin plomo que comprimen los sistemas de un solo componente en una pequeña cápsula que reside dentro del corazón .
Aplicación de un imán clínico a un marcapasos:
La colocación de un imán clínico sobre un marcapasos hace que el dispositivo pase a un modo asíncrono, normalmente VOO o DOO. Esto da lugar a un ritmo constante independientemente de la frecuencia o el ritmo nativo. Los imanes clínicos suelen tener una fuerza de ≥90 Gauss, muy superior a los 10 Gauss necesarios para alterar el funcionamiento del dispositivo. Si la aplicación del imán no produce ninguna respuesta en un ECG incluso después de reposicionarlo, considere el agotamiento de la batería, considere la posibilidad de añadir un segundo imán y considere que el marcapasos puede estar programado para ignorar el imán.
Esta característica es útil para evaluar la captura del marcapasos y evaluar la vida de la batería. El fallo de la batería puede excluirse si aparecen complejos de estimulación no presentes en el ECG de referencia cuando se aplica el imán . Un imán también puede utilizarse para interrumpir una taquicardia mediada por un marcapasos. Además, cuando se cree que la causa de una bradicardia inestable es la sobredetección, se puede colocar un imán sobre el dispositivo de marcapasos para cambiar su configuración, eliminando así cualquier función de detección y permitiendo la estimulación a una frecuencia predeterminada (normalmente 60-80 lpm). En los individuos obesos, puede ser necesario más de un imán.
Por último, con la excepción de los marcapasos Sorin, la retirada del imán hace que el dispositivo vuelva a marcar el ritmo normal preprogramado.
Para más FOAMed echa un vistazo a este post sobre los fundamentos del marcapasos en REBEL EM: http://rebelem.com/pacemaker-basics/
- Allison, Michael G., y H. A. Mallemat. Emergency Care of Patients with Pacemakers and Defibrillators. Clínicas de Medicina de Emergencia de América del Norte. 2015. 33(3). 653-667.
- Cardall, Taylor Y., et al. Permanent Cardiac Pacemakers: Issues Relevant to the Emergency Physician, Part I. The Journal of Emergency Medicine. 1999. 17(3). 479-489.
- Eifling, Michael, M. Razavi, y A. Massumi. La evaluación y el manejo de la tormenta eléctrica. Revista del Instituto del Corazón de Texas. 2011. 38(2). 111-121.
- Jacob, Sony, et al. Cardiac Rhythm Device Identification Algorithm Using X-rays: CaRDIA-X. Sociedad del ritmo cardíaco. 2011. 8(6). 915-922.
- Jacob, Sony, et al. Clinical Applications of Magnets on Cardiac Rhythm Management Devices. Europace. 2011. 13. 1222-1230.
- Madhavan, Malini, et al. Advances and Future Directions in Cardiac Pacemakers. Revista del Colegio Americano de Cardiología. 2017. 69(2). 211-235.
- McMullan, Jason, et al. Care of the Pacemaker/Implantable Cardioverter Defibrillator in the ED. American Journal of Emergency Medicine. 2007. 25. 812-822.
- Mulpuru, Siva, et al. Cardiac Pacemakers: Función, solución de problemas y manejo. Revista del Colegio Americano de Cardiología. 2017. 69(2). 189-210.
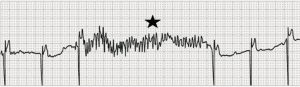
Superdetección de miopotencial e inhibición de la estimulación: La actividad del músculo esquelético se confunde con la actividad cardíaca (estrella) lo que provoca la inhibición de la estimulación en un paciente con un marcapasos programado en modo VVI.
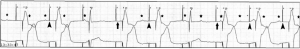
Superdetección y pérdida de captura: Las ondas P están marcadas con asteriscos. El infradetección (punta de flecha) se observa cuando una onda P es seguida brevemente por un pico de estimulación. La pérdida de captura (flecha) se observa cuando un pico de estimulación debidamente programado no genera una onda P.