Neurotossina
Come le neurotossine sono composti che influenzano negativamente il sistema nervoso, un certo numero di meccanismi attraverso i quali funzionano sono attraverso l’inibizione dei processi cellulari dei neuroni. Questi processi inibiti possono andare dai meccanismi di depolarizzazione della membrana alla comunicazione inter-neuronale. Inibendo la capacità dei neuroni di svolgere le loro funzioni intracellulari previste, o di passare un segnale a una cellula vicina, le neurotossine possono indurre un arresto del sistema nervoso sistemico, come nel caso della tossina botulinica, o addirittura la morte del tessuto nervoso. Il tempo necessario per la comparsa dei sintomi dopo l’esposizione alla neurotossina può variare tra le diverse tossine, essendo dell’ordine di ore per la tossina botulinica e di anni per il piombo.
| classificazione delle neurotossine | Neurotossine | |
|---|---|---|
| Inibitori dei canali Na | Tetrodotossina | |
| Inibitori del canale K | Tetraetilammonio | |
| Inibitori del canale Cl | Clorotossina, | |
| Inibitori dei canali Ca | Conotossina | |
| Inibitori del rilascio delle vescicole sinaptiche | Tossina botulinica, tossina tetanica | |
| Inibitori dei recettori | Bungarotossina
Curare |
|
| Agonisti dei recettori | 25I-NBOMe
JWH-0185-MEO-DiPT |
|
| Inibitori della barriera ematoencefalica | mercurio | |
| Interferenza del citoscheletro | Arsenico, ammoniaca | |
| Ca-citotossicità mediata | Piombo | |
| Effetti multipli | Etanolo&metanolo | |
| Fonti neurotossiche endogene | Ossido nitrico, Glutammato, Dopamina |
InhibitorsEdit
Sodium channelEdit
TetrodotoxinEdit

La tetrodotossina (TTX) è un veleno prodotto da organismi appartenenti all’ordine dei Tetraodontiformi, che comprende il pesce palla, il pesce luna oceanico e il pesce istrice. Nel pesce palla, la TTX si trova nel fegato, nelle gonadi, nell’intestino e nella pelle. Il TTX può essere fatale se consumato, ed è diventato una forma comune di avvelenamento in molti paesi. I sintomi comuni del consumo di TTX includono parestesia (spesso limitata alla bocca e agli arti), debolezza muscolare, nausea e vomito e spesso si manifestano entro 30 minuti dall’ingestione. Il meccanismo principale con cui la TTX è tossica è attraverso l’inibizione della funzione del canale del sodio, che riduce la capacità funzionale di comunicazione dei neuroni. Questa inibizione colpisce in gran parte un sottoinsieme suscettibile di canali del sodio noti come TTX-sensibili (TTX-s), che sono anche in gran parte responsabili della corrente di sodio che guida la fase di depolarizzazione dei potenziali d’azione dei neuroni.

TTX-resistente (TTX-r) è un’altra forma di canale del sodio che ha una sensibilità limitata al TTX, e si trova in gran parte in assoni di piccolo diametro come quelli trovati nei neuroni della nocicezione. Quando viene ingerito un livello significativo di TTX, esso lega i canali del sodio sui neuroni e riduce la loro permeabilità di membrana al sodio. Questo si traduce in un aumento della soglia effettiva dei segnali eccitatori richiesti per indurre un potenziale d’azione in un neurone postsinaptico. L’effetto di questa soglia di segnalazione aumentata è una ridotta eccitabilità dei neuroni postsinaptici e la conseguente perdita della funzione motoria e sensoriale che può portare alla paralisi e alla morte. Anche se la ventilazione assistita può aumentare le possibilità di sopravvivenza dopo l’esposizione al TTX, attualmente non esiste un’antitossina. L’uso dell’inibitore dell’acetilcolinesterasi Neostigmina o dell’antagonista muscarinico dell’acetilcolina Atropina (che inibisce l’attività parasimpatica), tuttavia, può aumentare l’attività del nervo simpatico abbastanza da migliorare le possibilità di sopravvivenza dopo l’esposizione al TTX.
Canale del potassioEdit
TetraetilammonioEdit
Il tetraetilammonio (TEA) è un composto che, come un certo numero di neurotossine, è stato identificato per la prima volta attraverso i suoi effetti dannosi al sistema nervoso e ha dimostrato di avere la capacità di inibire la funzione dei nervi motori e quindi la contrazione della muscolatura in modo simile a quella del curaro. Inoltre, attraverso la somministrazione cronica di TEA, verrebbe indotta l’atrofia muscolare. In seguito è stato determinato che la TEA funziona in vivo principalmente attraverso la sua capacità di inibire sia i canali del potassio responsabili del rettificatore ritardato visto in un potenziale d’azione sia alcune popolazioni di canali del potassio dipendenti dal calcio. È questa capacità di inibire il flusso di potassio nei neuroni che ha reso la TEA uno degli strumenti più importanti nelle neuroscienze. È stato ipotizzato che la capacità della TEA di inibire i canali del potassio derivi dalla sua struttura simile a quella degli ioni di potassio. Ciò che rende la TEA molto utile per i neuroscienziati è la sua capacità specifica di eliminare l’attività dei canali del potassio, permettendo così lo studio dei contributi di risposta del neurone di altri canali ionici come i canali del sodio gated al voltaggio. Oltre ai suoi molti usi nella ricerca neuroscientifica, TEA ha dimostrato di funzionare come un trattamento efficace del morbo di Parkinson attraverso la sua capacità di limitare la progressione della malattia.
Canale del cloruroModifica
ClorotossinaModifica
Chlorotoxin (Cltx) è il composto attivo trovato nel veleno dello scorpione, ed è principalmente tossico a causa della sua capacità di inibire la conduttanza dei canali del cloruro. L’ingestione di volumi letali di Cltx provoca la paralisi attraverso questa interruzione dei canali ionici. Simile alla tossina botulinica, il Cltx ha dimostrato di possedere un significativo valore terapeutico. L’evidenza ha dimostrato che il Cltx può inibire la capacità dei gliomi di infiltrarsi nel tessuto nervoso sano del cervello, riducendo significativamente il potenziale danno invasivo causato dai tumori.
Calcium channelEdit
ConotoxinEdit
Le conotossine rappresentano una categoria di veleni prodotti dalla lumaca marina cono, e sono in grado di inibire l’attività di una serie di canali ionici come i canali del calcio, sodio o potassio. In molti casi, le tossine rilasciate dai diversi tipi di lumache a cono includono una serie di diversi tipi di conotossine, che possono essere specifiche per diversi canali ionici, creando così un veleno capace di interruzione diffusa della funzione nervosa. Una delle forme uniche di conotossine, la ω-conotossina (ω-CgTx) è altamente specifica per i canali del Ca e ha dimostrato di essere utile per isolarli da un sistema. Poiché il flusso di calcio è necessario per la corretta eccitabilità di una cellula, qualsiasi inibizione significativa potrebbe impedire una grande quantità di funzionalità. Significativamente, ω-CgTx è in grado di legarsi a lungo termine e inibire i canali del calcio voltaggio-dipendenti situati nelle membrane dei neuroni ma non quelli delle cellule muscolari.
Rilascio delle vescicole sinapticheModifica
Tossina botulinicaModifica
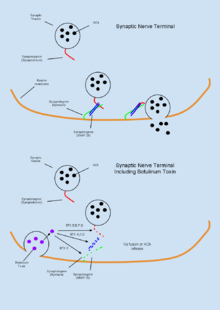
La tossina botulinica (BTX) è un gruppo di neurotossine composto da otto composti distinti, denominati BTX-A,B,C,D,E,F,G,H, che sono prodotti dal batterio Clostridium botulinum e provocano la paralisi muscolare. Una caratteristica unica del BTX è il suo uso terapeutico relativamente comune nel trattamento della distonia e dei disturbi della spasticità, così come nell’indurre l’atrofia muscolare, nonostante sia la sostanza più velenosa conosciuta. Il BTX funziona perifericamente per inibire il rilascio di acetilcolina (ACh) alla giunzione neuromuscolare attraverso la degradazione delle proteine SNARE necessarie per la fusione vescicola-membrana dell’ACh. Poiché la tossina è altamente biologicamente attiva, una dose stimata di 1μg/kg di peso corporeo è sufficiente per indurre un volume corrente insufficiente e la conseguente morte per asfissia. A causa della sua alta tossicità, le antitossine BTX sono state un’area attiva di ricerca. È stato dimostrato che la capsaicina (composto attivo responsabile del calore nel peperoncino) può legare il recettore TRPV1 espresso sui neuroni colinergici e inibire gli effetti tossici del BTX.
Tetanus toxinEdit
Tetanus neurotoxin (TeNT) è un composto che riduce funzionalmente le trasmissioni inibitorie nel sistema nervoso con conseguente tetania muscolare. TeNT è simile al BTX, ed è infatti molto simile per struttura e origine; entrambi appartengono alla stessa categoria di neurotossine clostridiali. Come il BTX, il TeNT inibisce la comunicazione tra i neuroni attraverso il rilascio di neurotrasmettitori vescicolari (NT). Una differenza notevole tra i due composti è che mentre il BTX inibisce le contrazioni muscolari, il TeNT le induce. Anche se entrambe le tossine inibiscono il rilascio di vescicole alle sinapsi dei neuroni, la ragione di questa diversa manifestazione è che il BTX funziona principalmente nel sistema nervoso periferico (PNS) mentre il TeNT è largamente attivo nel sistema nervoso centrale (CNS). Questo è il risultato della migrazione di TeNT attraverso i motoneuroni verso i neuroni inibitori del midollo spinale dopo essere entrato attraverso l’endocitosi. Questo si traduce in una perdita di funzione nei neuroni inibitori all’interno del SNC con conseguenti contrazioni muscolari sistemiche. Simile alla prognosi di una dose letale di BTX, TeNT porta alla paralisi e al successivo soffocamento.
Barriera ematoencefalicaModifica
AlluminioModifica
Il comportamento neurotossico dell’alluminio è noto per verificarsi all’entrata nel sistema circolatorio, dove può migrare al cervello e inibire alcune delle funzioni cruciali della barriera ematoencefalica (BBB). Una perdita di funzione nella BBB può produrre danni significativi ai neuroni nel SNC, come la barriera che protegge il cervello da altre tossine che si trovano nel sangue non sarà più in grado di tale azione. Anche se il metallo è noto per essere neurotossico, gli effetti sono di solito limitati ai pazienti incapaci di rimuovere gli ioni in eccesso dal sangue, come quelli che hanno un’insufficienza renale. I pazienti che sperimentano la tossicità dell’alluminio possono mostrare sintomi come l’apprendimento compromesso e la ridotta coordinazione motoria. Inoltre, i livelli sistemici di alluminio sono noti per aumentare con l’età e hanno dimostrato di essere correlati al morbo di Alzheimer, implicandolo come un composto neurotossico causale della malattia. Nonostante la sua nota tossicità, l’alluminio è ancora ampiamente utilizzato nell’imballaggio e nella preparazione degli alimenti, mentre altri metalli tossici come il piombo sono stati quasi completamente eliminati dall’uso in queste industrie.
MercuryEdit
Il mercurio è in grado di indurre danni al SNC migrando nel cervello attraversando la BBB. Il mercurio esiste in un certo numero di composti differenti, sebbene il metilmercurio (MeHg+), il dimetilmercurio e il dietilmercurio siano le uniche forme significativamente neurotossiche. Il dietilmercurio e il dimetilmercurio sono considerati alcune delle più potenti neurotossine mai scoperte. Il MeHg+ è solitamente acquisito attraverso il consumo di frutti di mare, poiché tende a concentrarsi in organismi alti nella catena alimentare. È noto che lo ione mercurico inibisce il trasporto degli aminoacidi (AA) e del glutammato (Glu), portando potenzialmente a effetti eccitotossici.
Agonisti e antagonisti del recettoreModifica
Anatossina-aEdit
Università di Nottingham
Indagini su anatossina-a, conosciuta anche come “Very Fast Death Factor”, è iniziata nel 1961 in seguito alla morte di mucche che avevano bevuto da un lago contenente una fioritura algale in Saskatchewan, Canada. Si tratta di una cianotossina prodotta da almeno quattro diversi generi di cianobatteri, ed è stata riportata in Nord America, Europa, Africa, Asia e Nuova Zelanda.
Gli effetti tossici dell’anatossina-a progrediscono molto rapidamente perché agisce direttamente sulle cellule nervose (neuroni). I sintomi progressivi dell’esposizione all’anatossina-a sono perdita di coordinazione, contrazioni, convulsioni e rapida morte per paralisi respiratoria. I tessuti nervosi che comunicano con i muscoli contengono un recettore chiamato recettore nicotinico dell’acetilcolina. La stimolazione di questi recettori causa una contrazione muscolare. La molecola di anatossina-a è modellata in modo da adattarsi a questo recettore, e in questo modo imita il neurotrasmettitore naturale normalmente usato dal recettore, l’acetilcolina. Una volta che ha innescato una contrazione, l’anatossina-a non permette ai neuroni di tornare al loro stato di riposo, perché non viene degradata dalla colinesterasi che normalmente svolge questa funzione. Di conseguenza, le cellule muscolari si contraggono permanentemente, la comunicazione tra il cervello e i muscoli è interrotta e la respirazione si ferma.
Quando fu scoperta per la prima volta, la tossina fu chiamata Very Fast Death Factor (VFDF) perché quando veniva iniettata nella cavità del corpo dei topi induceva tremori, paralisi e morte in pochi minuti. Nel 1977, la struttura del VFDF fu determinata come un alcaloide amminico secondario e biciclico, e fu rinominato anatossina-a. Strutturalmente, è simile alla cocaina. C’è un interesse continuo per l’anatossina-a a causa dei pericoli che presenta per le acque ricreative e potabili, e perché è una molecola particolarmente utile per studiare i recettori dell’acetilcolina nel sistema nervoso. La letalità della tossina significa che ha un alto potenziale militare come arma tossica.
BungarotoxinEdit
Bungarotoxin è un composto con interazione nota con i recettori nicotinici dell’acetilcolina (nAChRs), che costituiscono una famiglia di canali ionici la cui attività è attivata dal legame del neurotrasmettitore. La bungarotossina è prodotta in un certo numero di forme diverse, anche se una delle forme comunemente usate è la forma alfa a catena lunga, la α-bungarotossina, che è isolata dal serpente krait a bande. Sebbene sia estremamente tossica se ingerita, l’α-bungarotossina ha mostrato una grande utilità nelle neuroscienze in quanto è particolarmente adatta a isolare i nAChR a causa della sua alta affinità con i recettori. Poiché ci sono più forme di bungarotossina, ci sono diverse forme di nAChR a cui si legheranno, e l’α-bungarotossina è particolarmente specifica per α7-nAChR. Questo α7-nAChR funziona per consentire l’afflusso di ioni calcio nelle cellule, e quindi quando viene bloccato dalla bungarotossina ingerita produrrà effetti dannosi, poiché la segnalazione di ACh sarà inibita. Allo stesso modo, l’uso di α-bungarotossina può essere molto utile nelle neuroscienze se è desiderabile bloccare il flusso di calcio per isolare gli effetti di altri canali. Inoltre, diverse forme di bungarotossina possono essere utili per studiare i nAChR inibiti e il loro flusso di ioni calcio risultante in diversi sistemi del corpo. Per esempio, α-bungarotossina è specifico per nAChRs trovato nella muscolatura e κ-bungarotossina è specifico per nAChRs trovato in neuroni.
CaramboxinEdit
Caramboxin (CBX) è una tossina trovato in frutta stella (Averrhoa carambola). Gli individui con alcuni tipi di malattie renali sono suscettibili di effetti neurologici avversi tra cui intossicazione, convulsioni e persino la morte dopo aver mangiato la carambola o bevuto il succo di questo frutto. La caramboxina è una nuova tossina aminoacidica non peptidica che stimola i recettori del glutammato nei neuroni. La caramboxina è un agonista dei recettori ionotropi glutammatergici NMDA e AMPA con potenti proprietà eccitatorie, convulsive e neurodegenerative.
CurareEdit
Il termine “curare” è ambiguo perché è stato usato per descrivere una serie di veleni che al momento della denominazione erano intesi in modo diverso da quello attuale. In passato la caratterizzazione ha significato veleni usati dalle tribù sudamericane su frecce o dardi, anche se è maturato per specificare una categorizzazione specifica di veleni che agiscono sulla giunzione neuromuscolare per inibire la segnalazione e quindi indurre il rilassamento muscolare. La categoria delle neurotossine contiene un certo numero di veleni distinti, anche se tutti sono stati originariamente purificati da piante originarie del Sud America. L’effetto con cui il veleno del curaro iniettato è solitamente associato è la paralisi muscolare e la conseguente morte. Il curaro funziona in particolare per inibire i recettori nicotinici dell’acetilcolina alla giunzione neuromuscolare. Normalmente, questi canali recettori permettono agli ioni di sodio nelle cellule muscolari di iniziare un potenziale d’azione che porta alla contrazione muscolare. Bloccando i recettori, la neurotossina è in grado di ridurre significativamente la segnalazione della giunzione neuromuscolare, un effetto che ha portato al suo utilizzo da parte degli anestesisti per produrre il rilassamento muscolare.
Interferenza del citoscheletroModifica
ArsenicoModifica
L’arsenico è una neurotossina comunemente trovata concentrata in aree esposte al deflusso agricolo, alle miniere e ai siti di fusione (Martinez-Finley 2011). Uno degli effetti dell’ingestione di arsenico durante lo sviluppo del sistema nervoso è l’inibizione della crescita dei neuriti che può verificarsi sia nel PNS che nel CNS. Questa inibizione della crescita dei neuriti può spesso portare a difetti nella migrazione neurale, e significativi cambiamenti morfologici dei neuroni durante lo sviluppo,) spesso portando a difetti del tubo neurale nei neonati. Come metabolita dell’arsenico, l’arsenito si forma dopo l’ingestione di arsenico e ha mostrato una significativa tossicità per i neuroni entro circa 24 ore dall’esposizione. Il meccanismo di questa citotossicità funziona attraverso gli aumenti indotti dall’arsenite nei livelli intracellulari di ioni calcio nei neuroni, che possono successivamente ridurre il potenziale transmembrana mitocondriale che attiva le caspasi, innescando la morte cellulare. Un’altra funzione nota dell’arsenito è la sua natura distruttiva nei confronti del citoscheletro attraverso l’inibizione del trasporto dei neurofilamenti. Questo è particolarmente distruttivo in quanto i neurofilamenti sono utilizzati nella struttura e nel supporto delle cellule di base. La somministrazione di litio ha dimostrato di essere promettente, tuttavia, nel ripristinare parte della motilità dei neurofilamenti persa. Inoltre, simile ad altri trattamenti per le neurotossine, la somministrazione di alcuni antiossidanti ha mostrato qualche promessa nel ridurre la neurotossicità dell’arsenico ingerito.
AmmoniaEdit

La tossicità dell’ammoniaca è spesso vista attraverso due vie di somministrazione, o attraverso il consumo o attraverso disturbi endogeni come l’insufficienza epatica. Un caso degno di nota in cui la tossicità dell’ammoniaca è comune è in risposta alla cirrosi epatica che provoca un’encefalopatia epatica e può provocare un edema cerebrale (Haussinger 2006). Questo edema cerebrale può essere il risultato del rimodellamento delle cellule nervose. Come conseguenza dell’aumento delle concentrazioni, è stato dimostrato che l’attività dell’ammoniaca in vivo induce il gonfiore degli astrociti nel cervello attraverso l’aumento della produzione di cGMP (guanosina monofosfato ciclico) all’interno delle cellule che porta a modifiche del citoscheletro mediate dalla proteina chinasi G (PKG). L’effetto risultante di questa tossicità può essere un ridotto metabolismo energetico e funzione del cervello. È importante notare che gli effetti tossici dell’ammoniaca sul rimodellamento degli astrociti possono essere ridotti attraverso la somministrazione di L-carnitina. Questo rimodellamento degli astrociti sembra essere mediato dalla transizione di permeabilità mitocondriale indotta dall’ammoniaca. Questa transizione mitocondriale è un risultato diretto dell’attività della glutammina, un composto che si forma dall’ammoniaca in vivo. La somministrazione di antiossidanti o di un inibitore della glutaminasi può ridurre questa transizione mitocondriale, e potenzialmente anche il rimodellamento degli astrociti.
Citotossicità mediata dal calcioModifica

LeadEdit
Il piombo è una potente neurotossina la cui tossicità è stata riconosciuta da almeno migliaia di anni. Anche se gli effetti neurotossici del piombo si riscontrano sia negli adulti che nei bambini piccoli, il cervello in via di sviluppo è particolarmente suscettibile ai danni indotti dal piombo, effetti che possono includere apoptosi ed eccitotossicità. Un meccanismo sottostante con cui il piombo è in grado di causare danni è la sua capacità di essere trasportato dalle pompe calcio ATPasi attraverso la BBB, permettendo un contatto diretto con le fragili cellule del sistema nervoso centrale. La neurotossicità deriva dalla capacità del piombo di agire in modo simile agli ioni di calcio, in quanto il piombo concentrato porterà all’assorbimento cellulare del calcio che interrompe l’omeostasi cellulare e induce l’apoptosi. È questo aumento di calcio intracellulare che attiva la proteina chinasi C (PKC), che si manifesta come deficit di apprendimento nei bambini a seguito dell’esposizione precoce al piombo. Oltre a indurre l’apoptosi, il piombo inibisce la segnalazione degli interneuroni attraverso l’interruzione del rilascio di neurotrasmettitori mediato dal calcio.
Neurotossine con effetti multipliModifica
EtanoloModifica

Come neurotossina, è stato dimostrato che l’etanolo induce danni al sistema nervoso e colpisce il corpo in vari modi. Tra gli effetti noti dell’esposizione all’etanolo ci sono conseguenze sia transitorie che durature. Alcuni degli effetti duraturi includono la neurogenesi ridotta a lungo termine nell’ippocampo, l’atrofia cerebrale diffusa e l’infiammazione indotta nel cervello. Da notare che l’ingestione cronica di etanolo ha inoltre dimostrato di indurre la riorganizzazione dei costituenti della membrana cellulare, portando a un bilayer lipidico caratterizzato da un aumento delle concentrazioni di membrana di colesterolo e grassi saturi. Questo è importante perché il trasporto dei neurotrasmettitori può essere compromesso attraverso l’inibizione del trasporto vescicolare, con conseguente diminuzione della funzione della rete neurale. Un esempio significativo di ridotta comunicazione inter-neurone è la capacità dell’etanolo di inibire i recettori NMDA nell’ippocampo, con conseguente riduzione del potenziamento a lungo termine (LTP) e dell’acquisizione della memoria. È stato dimostrato che NMDA svolge un ruolo importante nel LTP e di conseguenza nella formazione della memoria. Con l’assunzione cronica di etanolo, tuttavia, la suscettibilità di questi recettori NMDA per indurre LTP aumenta nei neuroni mesolimbici della dopamina in un modo dipendente dall’inositolo 1,4,5-trifosfato (IP3). Questa riorganizzazione può portare alla citotossicità neuronale sia attraverso l’iperattivazione dei neuroni postsinaptici che attraverso la dipendenza indotta dal consumo continuo di etanolo. Inoltre, è stato dimostrato che l’etanolo riduce direttamente l’accumulo intracellulare di ioni calcio attraverso l’inibizione dell’attività del recettore NMDA, e quindi riduce la capacità del verificarsi di LTP.
In aggiunta agli effetti neurotossici dell’etanolo negli organismi maturi, l’ingestione cronica è in grado di indurre gravi difetti di sviluppo. Nel 1973 è stata dimostrata per la prima volta una connessione tra l’assunzione cronica di etanolo da parte delle madri e i difetti nella loro prole. Questo lavoro è stato responsabile della creazione della classificazione della sindrome alcolica fetale, una malattia caratterizzata da aberrazioni morfogenetiche comuni come difetti nella formazione cranio-facciale, nello sviluppo degli arti e nella formazione cardiovascolare. L’entità della neurotossicità dell’etanolo nei feti che porta alla sindrome fetale da alcol è stata dimostrata essere dipendente dai livelli di antiossidanti nel cervello come la vitamina E. Poiché il cervello fetale è relativamente fragile e suscettibile agli stress indotti, gravi effetti deleteri dell’esposizione all’alcol possono essere visti in aree importanti come l’ippocampo e il cervelletto. La gravità di questi effetti dipende direttamente dalla quantità e dalla frequenza del consumo di etanolo da parte della madre e dalla fase di sviluppo del feto. È noto che l’esposizione all’etanolo provoca una riduzione dei livelli di antiossidanti, una disfunzione mitocondriale (Chu 2007), e la successiva morte neuronale, apparentemente come risultato di una maggiore generazione di specie ossidative reattive (ROS). Questo è un meccanismo plausibile, in quanto vi è una ridotta presenza nel cervello fetale di enzimi antiossidanti come catalasi e perossidasi. A sostegno di questo meccanismo, la somministrazione di alti livelli di vitamina E nella dieta risulta in effetti neurotossici ridotti o eliminati indotti dall’etanolo nei feti.
n-HexaneEdit
n-Hexane è una neurotossina che è stata responsabile dell’avvelenamento di diversi lavoratori nelle fabbriche cinesi di elettronica negli ultimi anni.
Neurotossine recettore-selettiveModifica
MPP+Modifica
MPP+, il metabolita tossico dell’MPTP è una neurotossina selettiva che interferisce con la fosforilazione ossidativa nei mitocondri inibendo il complesso I, portando all’esaurimento dell’ATP e alla conseguente morte cellulare. Questo avviene quasi esclusivamente nei neuroni dopaminergici della substantia nigra, con conseguente presentazione di parkinsonismo permanente nei soggetti esposti 2-3 giorni dopo la somministrazione.
Fonti di neurotossine endogeneModifica
A differenza delle fonti più comuni di neurotossine che vengono acquisite dal corpo attraverso l’ingestione, le neurotossine endogene hanno origine ed esercitano i loro effetti in vivo. Inoltre, anche se la maggior parte dei veleni e delle neurotossine esogene raramente possiedono utili capacità in-vivo, le neurotossine endogene sono comunemente usate dal corpo in modi utili e sani, come l’ossido nitrico che è usato nella comunicazione cellulare. È spesso solo quando questi composti endogeni diventano altamente concentrati che portano ad effetti pericolosi.
Ossido nitricoModifica
Anche se l’ossido nitrico (NO) è comunemente usato dal sistema nervoso nella comunicazione e segnalazione inter-neuronale, può essere attivo nei meccanismi che portano all’ischemia nel cervello (Iadecola 1998). La neurotossicità dell’NO si basa sulla sua importanza nell’eccitotossicità da glutammato, poiché l’NO è generato in maniera calcio-dipendente in risposta all’attivazione NMDA mediata dal glutammato, che si verifica ad un tasso elevato nell’eccitotossicità da glutammato. Anche se NO facilita l’aumento del flusso sanguigno nelle regioni potenzialmente ischemiche del cervello, è anche in grado di aumentare lo stress ossidativo, inducendo danni al DNA e apoptosi. Così una maggiore presenza di NO in un’area ischemica del SNC può produrre effetti significativamente tossici.
GlutammatoModifica
Il glutammato, come l’ossido nitrico, è un composto prodotto endogenamente usato dai neuroni per funzionare normalmente, essendo presente in piccole concentrazioni nella materia grigia del SNC. Uno degli usi più notevoli del glutammato endogeno è la sua funzionalità come neurotrasmettitore eccitatorio. Quando è concentrato, tuttavia, il glutammato diventa tossico per i neuroni circostanti. Questa tossicità può essere sia il risultato della letalità diretta del glutammato sui neuroni sia il risultato del flusso di calcio indotto nei neuroni che porta al gonfiore e alla necrosi. È stato dimostrato che questi meccanismi giocano un ruolo significativo in malattie e complicazioni come la malattia di Huntington, l’epilessia e l’ictus.
DopaminaModifica
La dopamina è un composto endogeno che viene utilizzato come neurotrasmettitore per modulare l’aspettativa di ricompensa. La dopamina uccide i neuroni produttori di dopamina interferendo con la catena di trasporto degli elettroni nei neuroni. Questa interferenza si traduce in un’inibizione della respirazione cellulare, portando alla morte dei neuroni.