Waarom geleiden metalen warmte en elektriciteit zo goed? Welke metalen geleiden het best?
Structuur van metalen
De structuur van zuivere metalen is eenvoudig te beschrijven, omdat de atomen die deze metalen vormen kunnen worden beschouwd als identieke perfecte bollen. Meer specifiek bestaat de metaalstructuur uit “uitgelijnde positieve ionen” (kationen) in een “zee” van gedelokaliseerde elektronen. Dit betekent dat de elektronen vrij door de structuur kunnen bewegen, waardoor eigenschappen als geleidbaarheid ontstaan.
Wat zijn de verschillende soorten bindingen?
Covalente bindingen
Een covalente binding is een binding die wordt gevormd wanneer twee atomen elektronen delen. Voorbeelden van verbindingen met covalente bindingen zijn water, suiker en koolstofdioxide.
Ionische bindingen
Ionische bindingen zijn de volledige overdracht van valentie-elektron(en) tussen een metaal en een niet-metaal. Dit resulteert in twee tegengesteld geladen ionen die elkaar aantrekken. In ionische bindingen verliest het metaal elektronen om een positief geladen kation te worden, terwijl het niet-metaal die elektronen aanvaardt om een negatief geladen anion te worden. Een voorbeeld van een Ionische binding is zout (NaCl).
Metallische bindingen
Metallische bindingen zijn het resultaat van de elektrostatische aantrekkingskracht die optreedt tussen geleidingselektronen (in de vorm van een elektronenwolk van gedelokaliseerde elektronen) en positief geladen metaalionen. Het kan worden omschreven als het delen van vrije elektronen onder een rooster van positief geladen ionen (kationen). De metaalbinding verklaart vele fysische eigenschappen van metalen, zoals sterkte, rekbaarheid, thermische en elektrische weerstand en geleidingsvermogen, opaciteit, en glans.
Gelokaliseerde bewegende elektronen in metalen —
Het is de vrije beweging van elektronen in metalen die hen hun geleidingsvermogen geven.
Elektrisch geleidingsvermogen
Metalen bevatten vrij bewegende gedelokaliseerde elektronen. Wanneer een elektrische spanning wordt toegepast, brengt een elektrisch veld in het metaal de beweging van de elektronen op gang, waardoor zij van het ene uiteinde van de geleider naar het andere uiteinde verschuiven. Elektronen zullen naar de positieve kant bewegen.
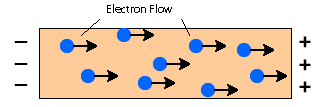
Warmtegeleiding
Metaal is een goede geleider van warmte. Geleiding vindt plaats wanneer een stof wordt verhit, deeltjes zullen meer energie krijgen, en meer gaan trillen. Deze moleculen botsen dan tegen naburige deeltjes en dragen een deel van hun energie aan hen over. Dit gaat dan verder en geeft de energie van het hete uiteinde door aan het koudere uiteinde van de stof.
Waarom geleiden metalen de warmte zo goed?
De elektronen in metalen zijn gedelokaliseerde elektronen en zijn vrij bewegende elektronen, dus als ze energie (warmte) krijgen, trillen ze sneller en kunnen ze zich sneller verplaatsen, waardoor ze de energie sneller kunnen doorgeven.
Welke metalen geleiden het best?
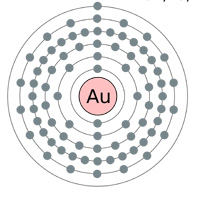
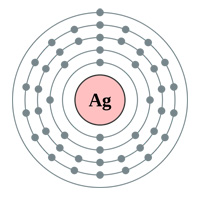
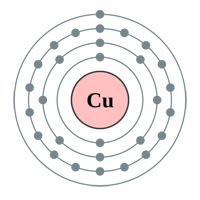
Boven: Elektronenschillen Goud (au), Zilver (Ag), Koper (Cu) en Zink (Zn). Logischerwijs zou men denken dat goud de beste geleider is, met een enkel elektron in de laatste schil (bovenstaande tabel) … dus waarom zijn zilver en koper eigenlijk beter (zie tabel hieronder).
|
Geleidbaarheid van metalen
|
>S/m
|
Zilver | 6.30×10 7 |
| Koper | 5,96×10 7 |
| Goud | 4.10×10 7 |
| Aluminium | 3,50×10 7 |
| Zink | 1.69×10 7 |
Zilver heeft een grotere atomaire straal (160 pm) dan goud (135 pm), ondanks het feit dat goud meer elektronen heeft dan zilver! Voor een reden hiervoor zie het commentaar hieronder.
Opmerking: Zilver is een betere geleider dan goud, maar goud is meer gewild omdat het niet corrodeert. (Koper is de meest voorkomende omdat het de meest kosteneffectieve) Het antwoord is een beetje ingewikkeld en we site hier een van de beste antwoorden die we hebben gezien voor degenen die bekend zijn met het materiaal.
“Zilver zit in het midden van de transistionele metalen, ongeveer halverwege tussen de edelgassen en de alkalimetalen. In kolom 11 van het periodiek systeem hebben al deze elementen (koper, zilver en goud) een enkel s-orbitaal elektron in de buitenste schil (platina heeft dat ook, in kolom 10).
De baanstructuur van de elektronen van deze elementen heeft geen bijzondere affiniteit om een elektron te winnen of een elektron te verliezen ten opzichte van de edelgassen die zwaarder of lichter zijn, omdat ze er 1/2 tussenin zitten. In het algemeen betekent dit dat er niet veel energie nodig is om tijdelijk een elektron af te stoten of tijdelijk een toe te voegen. De specifieke elektronenaffiniteiten en ionisatiepotentiëlen lopen uiteen, en wat geleiding betreft is het hebben van relatief lage energieën voor deze twee criteria enigszins belangrijk.
Als dat de enige criteria waren, dan zou goud een betere geleider zijn dan zilver, maar goud heeft 14 extra f-hoofdplaat elektronen naast de 10 d-hoofdplaat elektronen en het enkele s-hoofdplaat elektron. De 14 f-elektronen zijn het gevolg van de extra atomen in de actinidereeks. Met 14 extra elektronen die blijkbaar op de d- en s-elektronen drukken, zou je denken dat het s-elektron daar gewoon ‘rijp’ was voor geleiding (er was nauwelijks energie nodig om het eraf te stoten), maar NOOO. De elektronen in de f-hoofdschil zitten zo opeengepakt dat de atomaire straal van goud in feite KLEINER is dan de atomaire straal van zilver — niet veel, maar het is kleiner. Een kleinere straal betekent meer kracht van de kern op de buitenste elektronen, dus zilver wint in de geleidingswedstrijd. Vergeet niet dat de kracht van de elektrische lading omgekeerd evenredig is met het kwadraat van de afstand. Hoe dichter 2 ladingen bij elkaar zijn, hoe groter de kracht tussen hen.
Koper en platina hebben zelfs nog kleinere diameters; vandaar meer aantrekkingskracht van de kern, vandaar meer energie om dat eenzame s-elektron af te stoten, vandaar een lager geleidingsvermogen.
Andere elementen met een enkel s-orbitaal elektron “rijp voor de geleider om langs te komen”, hebben ook lagere atomaire stralen (molybdeen, niobium, chromium, ruthenium, rhodium) dan zilver.
Dus, het is vooral waar het zit — waar ‘moeder natuur’ zilver in het periodiek systeem heeft geplaatst, dat zijn uitstekende geleidingsvermogen dicteert.”
Bron van tlbs101 Yahoo