Cos’è il vapore?
Proprietà del vapore
Una migliore comprensione delle proprietà del vapore può essere raggiunta comprendendo la struttura molecolare e atomica generale della materia, e applicando questa conoscenza a ghiaccio, acqua e vapore.
Una molecola è la più piccola quantità di qualsiasi elemento o sostanza composta che possiede ancora tutte le proprietà chimiche di quella sostanza che può esistere. Le molecole stesse sono formate da particelle ancora più piccole chiamate atomi, che definiscono gli elementi di base come l’idrogeno e l’ossigeno.
Le combinazioni specifiche di questi elementi atomici forniscono sostanze composte. Uno di questi composti è rappresentato dalla formula chimica H2O, con molecole formate da due atomi di idrogeno e un atomo di ossigeno.

La ragione per cui l’acqua è così abbondante sulla terra è che l’idrogeno e l’ossigeno sono tra gli elementi più abbondanti nell’universo. Il carbonio è un altro elemento di notevole abbondanza, ed è un componente chiave in tutta la materia organica.
La maggior parte delle sostanze minerali può esistere nei tre stati fisici (solido, liquido e vapore) che vengono chiamati fasi. Nel caso dell’H2O, i termini ghiaccio, acqua e vapore sono usati per indicare rispettivamente le tre fasi.
La disposizione molecolare del ghiaccio, dell’acqua e del vapore non è ancora del tutto compresa, ma è conveniente considerare le molecole come legate insieme da cariche elettriche (definite come legame idrogeno).
Il grado di eccitazione delle molecole determina lo stato fisico (o fase) della sostanza.
Punto triplo
Tutte le tre fasi di una particolare sostanza possono coesistere in equilibrio solo ad una certa temperatura e pressione, e questo è noto come il suo punto triplo.
Il punto triplo di H2O, dove le tre fasi di ghiaccio, acqua e vapore sono in equilibrio, si verifica ad una temperatura di 273,16 K e una pressione assoluta di 0,006 112 bar. Questa pressione è molto vicina al vuoto perfetto. Se la pressione viene ridotta ulteriormente a questa temperatura, il ghiaccio, invece di sciogliersi, sublima direttamente in vapore.
Ghiaccio
Nel ghiaccio, le molecole sono bloccate insieme in una struttura ordinata tipo reticolo e possono solo vibrare. Nella fase solida, il movimento delle molecole nel reticolo è una vibrazione intorno a una posizione media di legame in cui le molecole sono a meno di un diametro molecolare l’una dall’altra.
L’aggiunta continua di calore fa sì che la vibrazione aumenti a tal punto che alcune molecole alla fine si staccheranno dai loro vicini, e il solido inizia a sciogliersi allo stato liquido. A pressione atmosferica, la fusione avviene a 0°C. I cambiamenti di pressione hanno un effetto molto piccolo sulla temperatura di fusione, e per la maggior parte degli scopi pratici, 0°C può essere preso come punto di fusione. Tuttavia, è stato dimostrato che il punto di fusione del ghiaccio diminuisce di 0,0072°C per ogni atmosfera aggiuntiva di pressione. Per esempio, una pressione di 13,9 bar g sarebbe necessaria per ridurre la temperatura di fusione di 0,1°C.
Il calore che rompe i legami reticolari per produrre il cambiamento di fase, mentre non aumenta la temperatura del ghiaccio, è indicato come entalpia di fusione o calore di fusione. Questo fenomeno di cambiamento di fase è reversibile quando si verifica il congelamento con la stessa quantità di calore che viene rilasciata nuovamente nell’ambiente circostante.
Per la maggior parte delle sostanze, la densità diminuisce quando si passa dalla fase solida a quella liquida. Tuttavia, l’H2O è un’eccezione a questa regola, poiché la sua densità aumenta quando si scioglie, ed è per questo che il ghiaccio galleggia sull’acqua.
Acqua
Nella fase liquida, le molecole sono libere di muoversi, ma sono ancora a meno di un diametro molecolare a causa dell’attrazione reciproca, e le collisioni avvengono frequentemente. Più calore aumenta l’agitazione molecolare e la collisione, aumentando la temperatura del liquido fino alla sua temperatura di ebollizione.
Enthalpy of water, liquid enthalpy or sensible heat (hf) of water
Questa è l’energia termica richiesta per aumentare la temperatura dell’acqua da un punto di riferimento di 0°C alla sua temperatura attuale.
A questo stato di riferimento di 0°C, l’entalpia dell’acqua è stata arbitrariamente messa a zero. L’entalpia di tutti gli altri stati può quindi essere identificata rispetto a questo stato di riferimento facilmente accessibile.
Il calore sensibile era il termine usato una volta, perché il calore aggiunto all’acqua produceva un cambiamento di temperatura. Tuttavia, i termini accettati oggi sono entalpia liquida o entalpia dell’acqua.
A pressione atmosferica (0 bar g), l’acqua bolle a 100°C, e sono necessari 419 kJ di energia per riscaldare 1 kg di acqua da 0°C alla sua temperatura di ebollizione di 100°C. È da queste cifre che si ricava il valore della capacità termica specifica dell’acqua (Cp) di 4,19 kJ/kg °C per la maggior parte dei calcoli tra 0°C e 100°C.
Vapore
Come la temperatura aumenta e l’acqua si avvicina alla condizione di ebollizione, alcune molecole raggiungono abbastanza energia cinetica per raggiungere velocità che permettono loro di fuggire momentaneamente dal liquido nello spazio sopra la superficie, prima di ricadere nel liquido.
Un ulteriore riscaldamento causa una maggiore eccitazione e il numero di molecole con abbastanza energia per lasciare il liquido aumenta. Quando l’acqua viene riscaldata fino al suo punto di ebollizione, si formano al suo interno delle bolle di vapore che salgono fino a sfondare la superficie.
Considerando la disposizione molecolare dei liquidi e dei vapori, è logico che la densità del vapore sia molto inferiore a quella dell’acqua, perché le molecole di vapore sono più distanti tra loro. Lo spazio immediatamente sopra la superficie dell’acqua si riempie quindi di molecole di vapore meno dense.
Quando il numero di molecole che lasciano la superficie del liquido è maggiore di quelle che rientrano, l’acqua evapora liberamente. A questo punto ha raggiunto il punto di ebollizione o la sua temperatura di saturazione, poiché è satura di energia termica.
Se la pressione rimane costante, l’aggiunta di altro calore non fa aumentare ulteriormente la temperatura, ma fa sì che l’acqua formi vapore saturo. La temperatura dell’acqua bollente e del vapore saturo all’interno dello stesso sistema è la stessa, ma l’energia termica per unità di massa è molto maggiore nel vapore.
Alla pressione atmosferica la temperatura di saturazione è di 100°C. Tuttavia, se la pressione viene aumentata, questo permetterà l’aggiunta di più calore e un aumento della temperatura senza un cambiamento di fase.
Quindi, aumentando la pressione aumenta effettivamente sia l’entalpia dell’acqua, sia la temperatura di saturazione. La relazione tra la temperatura di saturazione e la pressione è nota come la curva di saturazione del vapore (vedi immagine qui sotto).
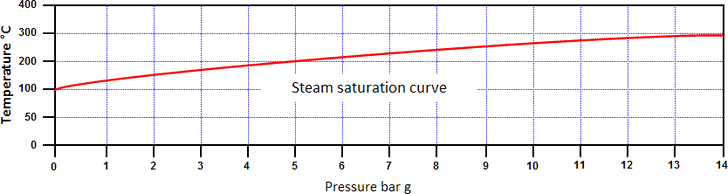
Acqua e vapore possono coesistere a qualsiasi pressione su questa curva, essendo entrambi alla temperatura di saturazione. Il vapore in una condizione al di sopra della curva di saturazione è conosciuto come vapore surriscaldato:
- La temperatura al di sopra della temperatura di saturazione è chiamata grado di surriscaldamento del vapore.
- L’acqua in una condizione al di sotto della curva è chiamata acqua sottosatura.
Se il vapore può uscire dalla caldaia alla stessa velocità con cui viene prodotto, l’aggiunta di ulteriore calore aumenta semplicemente il tasso di produzione. Se si impedisce al vapore di uscire dalla caldaia e si mantiene il tasso di ingresso del calore, l’energia che entra nella caldaia sarà maggiore di quella che esce. Questa energia in eccesso aumenta la pressione, permettendo a sua volta alla temperatura di saturazione di aumentare, poiché la temperatura del vapore saturo è correlata alla sua pressione.
Enthalpy of evaporation or latent heat (hfg)
Questa è la quantità di calore richiesta per cambiare lo stato dell’acqua alla sua temperatura di ebollizione, in vapore. Non comporta alcun cambiamento nella temperatura della miscela vapore/acqua, e tutta l’energia è usata per cambiare lo stato da liquido (acqua) a vapore (vapore saturo).
Il vecchio termine calore latente si basa sul fatto che, sebbene sia stato aggiunto calore, non c’è stato alcun cambiamento di temperatura. Tuttavia, il termine accettato ora è entalpia di evaporazione.
Come il cambiamento di fase dal ghiaccio all’acqua, anche il processo di evaporazione è reversibile. La stessa quantità di calore che ha prodotto il vapore viene rilasciata di nuovo nell’ambiente circostante durante la condensazione, quando il vapore incontra qualsiasi superficie a una temperatura inferiore.
Questo può essere considerato come la porzione utile di calore nel vapore per scopi di riscaldamento, poiché è quella porzione del calore totale nel vapore che viene estratta quando il vapore condensa di nuovo in acqua.
Enthalpy of saturated steam, or total heat of saturated steam
This is the total energy in saturated steam, and is simply the sum of the enthalpy of water and the enthalpy of evaporation.
hg = hf + hfg
- hg = Entalpia totale del vapore saturo (calore totale) (kJ/kg)
- hf = Entalpia del liquido (calore sensibile) (kJ/kg)
- hfg = Entalpia di evaporazione (calore latente) (kJ/kg)
Tabella del vapore saturo
Una tabella del vapore elenca le proprietà del vapore a varie pressioni. Sono i risultati di test reali effettuati sul vapore. La tabella qui sotto mostra le proprietà del vapore saturo secco alla pressione atmosferica – da 0 barg a 5 barg.
| Pressione barg |
Sat- durata temp °C |
Enthalpy (energia) in kJ/kg | Volume di vapore secco saturo m3/kg |
||
| Acqua hf | Eva- società hfg |
Vapore hg | |||
| 0 | 100 | 419 | 2257 | 2676 | 1.673 |
| 1 | 120 | 506 | 2201 | 2707 | 0.881 |
| 2 | 134 | 562 | 2163 | 2725 | 0.603 |
| 3 | 144 | 605 | 2133 | 2738 | 0.461 |
| 4 | 152 | 641 | 2108 | 2749 | 0.374 |
| 5 | 159 | 671 | 2086 | 2757 | 0.315 |
Frazioni di secchezza
Il vapore con una temperatura uguale al punto di ebollizione a quella pressione è noto come vapore saturo secco. Tuttavia, produrre il 100% di vapore secco in una caldaia industriale progettata per produrre vapore saturo è raramente possibile, e il vapore di solito contiene goccioline d’acqua.
In pratica, a causa della turbolenza e degli spruzzi, quando le bolle di vapore sfondano la superficie dell’acqua, lo spazio del vapore contiene una miscela di goccioline d’acqua e vapore.
Il vapore prodotto in qualsiasi caldaia a guscio, dove il calore viene fornito solo all’acqua e dove il vapore rimane in contatto con la superficie dell’acqua, può contenere tipicamente circa il 5% di acqua in massa.
Se il contenuto d’acqua del vapore è del 5‰ in massa, allora si dice che il vapore è secco al 95% e ha una frazione di secchezza dello 0,95.
L’entalpia effettiva di evaporazione del vapore umido è il prodotto della frazione di secchezza (X) e l’entalpia specifica (hfg) dalle tabelle del vapore. Il vapore umido avrà un’energia termica utilizzabile inferiore a quella del vapore saturo secco.
Entalpia effettiva di evaporazione = hfgX
Pertanto:
Entalpia totale effettiva = hf + hfgX
Perché il volume specifico dell’acqua è diversi ordini di grandezza inferiore a quello del vapore, le gocce d’acqua nel vapore umido occuperanno uno spazio trascurabile. Quindi il volume specifico del vapore umido sarà inferiore a quello del vapore secco:
Volume specifico effettivo = VgX
dove Vg è il volume specifico del vapore saturo secco.
Il diagramma di fase del vapore
I dati forniti nelle tabelle del vapore possono essere espressi anche in forma grafica. L’immagine qui sotto illustra la relazione tra l’entalpia e la temperatura dei vari stati dell’acqua e del vapore; questo è noto come diagramma di fase.
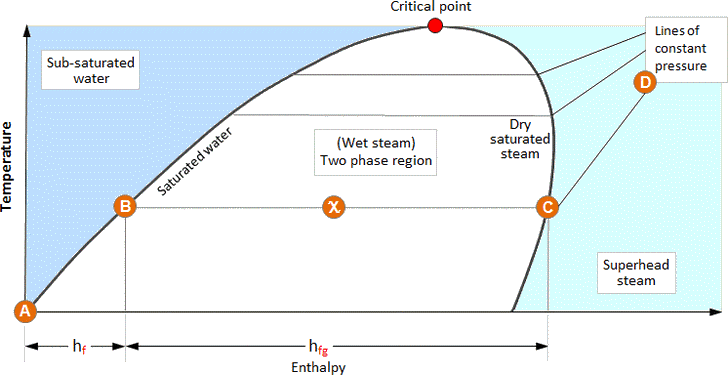
Quando l’acqua viene riscaldata da 0°C alla sua temperatura di saturazione, il suo stato segue la linea dell’acqua satura fino a quando ha ricevuto tutta la sua entalpia liquida, hf (A – B).
Se si continua ad aggiungere calore, l’acqua cambia fase in una miscela acqua/vapore e continua ad aumentare l’entalpia rimanendo alla temperatura di saturazione, hfg (B – C).
Come la miscela acqua/vapore aumenta in secchezza, la sua condizione si sposta dalla linea del liquido saturo alla linea del vapore saturo. Quindi in un punto esattamente a metà strada tra questi due stati, la frazione di secchezza (X) è 0,5. Allo stesso modo, sulla linea del vapore saturo il vapore è secco al 100%.
Una volta che ha ricevuto tutta la sua entalpia di evaporazione, raggiunge la linea del vapore saturo. Se continua ad essere riscaldato dopo questo punto, la pressione rimane costante, ma la temperatura del vapore comincerà ad aumentare per effetto del surriscaldamento (C – D).
Le linee dell’acqua satura e del vapore saturo racchiudono una regione in cui esiste una miscela acqua/vapore – vapore umido. Nella regione a sinistra della linea dell’acqua satura esiste solo acqua, e nella regione a destra della linea del vapore saturo esiste solo vapore surriscaldato.
Il punto in cui le linee dell’acqua satura e del vapore saturo si incontrano è conosciuto come il punto critico. Come la pressione aumenta verso il punto critico, l’entalpia di evaporazione diminuisce, fino a diventare zero nel punto critico. Questo suggerisce che l’acqua si trasforma direttamente in vapore saturo al punto critico.
Al di sopra del punto critico il vapore può essere considerato come un gas. Lo stato gassoso è lo stato più diffuso in cui le molecole hanno un movimento quasi illimitato, e il volume aumenta senza limiti man mano che la pressione si riduce.
Il punto critico è la temperatura più alta alla quale l’acqua può esistere. Qualsiasi compressione a temperatura costante al di sopra del punto critico non produrrà un cambiamento di fase.
La compressione a temperatura costante al di sotto del punto critico, tuttavia, provocherà la liquefazione del vapore mentre passa dalla regione surriscaldata alla regione del vapore umido.
Il punto critico si verifica a 374,15°C e 221,2 bar a per il vapore. Al di sopra di questa pressione il vapore è definito supercritico e non esiste un punto di ebollizione ben definito.
Vapore flash
Il termine “vapore flash” è tradizionalmente usato per descrivere il vapore che esce dagli sfiati del ricevitore di condensa e dalle linee di scarico della condensa aperte dalle trappole del vapore. Come può formarsi il vapore dall’acqua senza l’aggiunta di calore?
Il vapore istantaneo si verifica ogni volta che l’acqua ad alta pressione (e una temperatura superiore alla temperatura di saturazione del liquido a bassa pressione) viene lasciata cadere ad una pressione inferiore. Al contrario, se la temperatura dell’acqua ad alta pressione è inferiore alla temperatura di saturazione alla pressione inferiore, il flash steam non può formarsi. Nel caso della condensa che passa attraverso una trappola per il vapore, di solito la temperatura a monte è abbastanza alta da formare il flash steam. Vedi l’immagine qui sotto
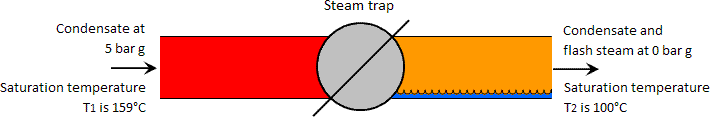
Consideriamo un chilogrammo di condensato a 5 bar g e una temperatura di saturazione di 159°C che passa attraverso una trappola per il vapore a una pressione inferiore di 0 bar g. La quantità di energia in un chilogrammo di condensato alla temperatura di saturazione a 5 bar g è 671 kJ. In accordo con la prima legge della termodinamica, la quantità di energia contenuta nel fluido dal lato della bassa pressione della trappola del vapore deve essere uguale a quella dal lato dell’alta pressione, e costituisce il principio di conservazione dell’energia.
Di conseguenza, il calore contenuto in un chilogrammo di fluido a bassa pressione è anche 671 kJ. Tuttavia, l’acqua a 0 bar g è in grado di contenere solo 419 kJ di calore, quindi sembra esserci uno squilibrio di calore sul lato a bassa pressione di 671 – 419 = 252 kJ, che, per quanto riguarda l’acqua, potrebbe essere considerato come calore in eccesso.
Questo calore in eccesso fa bollire parte del condensato in quello che è noto come vapore flash e il processo di ebollizione è chiamato flashing. Quindi, il chilogrammo di condensato che esisteva come un chilogrammo di acqua liquida sul lato dell’alta pressione della trappola del vapore ora esiste parzialmente sia come acqua che come vapore sul lato della bassa pressione.
La quantità di vapore flash prodotta alla pressione finale (P2) può essere determinata usando:
Proporzione di vapore flash = (hf a P1) – (hf a P2) / hfg a P2
- P1 = Pressione iniziale
- P2 = Pressione finale
- hf = Entalpia del liquido (kJ/kg)
- hfg = Entalpia di evaporazione (kJ/kg)
Esempio: Il caso in cui la temperatura di condensazione ad alta pressione è superiore alla temperatura di saturazione a bassa pressione.
Consideriamo una quantità di acqua ad una pressione di 5 bar g, contenente 671 kJ/kg di energia termica alla sua temperatura di saturazione di 159°C. Se la pressione fosse poi ridotta alla pressione atmosferica (0 bar g), l’acqua potrebbe esistere solo a 100°C e contenere 419 kJ/kg di energia termica. Questa differenza di 671 – 419 = 252 kJ/kg di energia termica, produrrebbe quindi vapore flash a pressione atmosferica.
670,9 – 419,0
2257,0
670.9 – 419,0
0,11 kg di vapore / kg di acqua
La proporzione di vapore flash prodotto può essere pensata come il rapporto tra l’energia in eccesso e l’entalpia di evaporazione alla pressione finale.
Esempio: Il caso in cui la temperatura del condensato ad alta pressione è inferiore alla temperatura di saturazione a bassa pressione.
La temperatura è a 90°C, cioè sottoraffreddata sotto la temperatura di saturazione atmosferica di 100°C. Nota: di solito non è pratico per un calo così grande della temperatura del condensato dalla sua temperatura di saturazione (in questo caso 159°C a 90°C); viene semplicemente usato per illustrare il punto sul fatto che il flash steam non viene prodotto in tali circostanze.
In questo caso, la tabella dell’acqua sub-satura mostrerà che l’entalpia liquida di un chilogrammo di condensato a 5 barg e 90°C è 377 kJ. Poiché questa entalpia è inferiore all’entalpia di un chilogrammo di acqua satura a pressione atmosferica (419 kJ), non c’è calore in eccesso disponibile per produrre vapore flash. Il condensato passa semplicemente attraverso la trappola e rimane allo stato liquido alla stessa temperatura ma a una pressione inferiore, la pressione atmosferica in questo caso. Vedi l’immagine qui sotto.
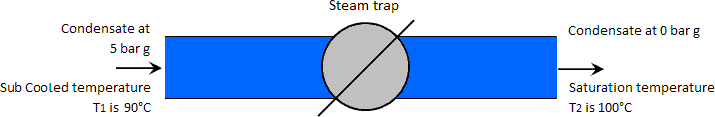
La pressione del vapore dell’acqua a 90°C è di 0,7 bar assoluti. Se la pressione inferiore della condensa fosse stata inferiore a questa, si sarebbe prodotto vapore istantaneo.
I principi di conservazione dell’energia e della massa tra due stati del processo.
I principi di conservazione dell’energia e della massa permettono di pensare al fenomeno del vapore istantaneo da una direzione diversa.
1 kg di condensa a 5 bar g e 159°C produce 0,112 kg di vapore istantaneo a pressione atmosferica. Questo può essere illustrato schematicamente nella tabella qui sotto. La massa totale di flash e condensato rimane 1 kg.
1 kg di condensato
159°C
Enthalpy 671 kJ
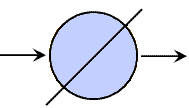
0.112 vapore flash
0,888 condensato
Il principio di conservazione dell’energia afferma che l’energia totale nello stato di pressione inferiore deve essere uguale all’energia totale nello stato di pressione superiore. Pertanto, la quantità di calore nel vapore e nel condensato flash deve essere uguale a quella nel condensato iniziale di 671 kJ.
Le tabelle del vapore danno le seguenti informazioni:
- Entalpia totale dell’acqua satura alla pressione atmosferica (hf) = 419 kJ/kg
- Entalpia totale nel vapore saturo alla pressione atmosferica (hg) = 2 675 kJ/kg
- Quindi, allo stato di pressione inferiore di 0 bar g
- Entalpia totale nell’acqua = 0.888 kg x 419 kJ / kg = 372 kJ (A)
- Entalpia totale nel vapore = 0.112 kg x 2 675 kJ / kg = 299 kJ (B)
- Entalpia totale nel condensato e nel vapore alla pressione inferiore = A + B = 671 kJ
Quindi, le tabelle del vapore, l’entalpia prevista nello stato di pressione inferiore è la stessa di quella nello stato di pressione superiore, dimostrando così il principio di conservazione dell’energia.
Generale
Vapore saturo
Il vapore è vapore acqueo. Ad una data temperatura c’è una certa pressione del vapore che esiste in equilibrio con l’acqua liquida. Questo è il vapore “umido” o saturo. Se la temperatura del vapore supera la temperatura alla quale è in equilibrio con una data pressione di vapore acqueo, il vapore è surriscaldato (riscaldato al di sopra della temperatura corrispondente alla pressione del vapore in equilibrio) e il vapore è detto “secco”. Conoscendo la pressione, si conosce anche la temperatura.
Vapore surriscaldato
Se il vapore saturo viene ulteriormente riscaldato, l’umidità diminuisce. Le goccioline d’acqua rimanenti sono più piccole e passano alla fase vapore. A temperature di 10-20°C al di sopra della temperatura del vapore saturo si è verificato un surriscaldamento.
A causa dello scarso trasferimento di calore il vapore surriscaldato è migliore per il trasporto di calore (flusso di vapore in lunghe condutture).
A causa del buon trasferimento di calore il vapore saturo è migliore per il trasferimento di calore (riscaldamento degli scambiatori di calore si dovrebbe usare il vapore saturo).
Vapore fresco
Il vapore fresco viene rilasciato dal condensato caldo quando la sua pressione viene ridotta. Anche l’acqua a una temperatura ambiente di 20°C bollirebbe se la sua pressione fosse abbassata abbastanza. Vale la pena notare che l’acqua a 170°C bollirà a qualsiasi pressione inferiore a 6,9 bar g. Il vapore rilasciato dal processo di flashing è utile quanto il vapore rilasciato da una caldaia a vapore.
Per esempio, quando il vapore viene prelevato da una caldaia e la pressione della caldaia scende, una parte dell’acqua contenuta nella caldaia verrà rilasciata in flash per integrare il vapore “vivo” prodotto dal calore del combustibile della caldaia. Poiché entrambi i tipi di vapore sono prodotti nella caldaia, è impossibile distinguerli. Solo quando il flashing avviene a una pressione relativamente bassa, come sul lato di scarico delle trappole del vapore, il termine flash steam è ampiamente utilizzato. Sfortunatamente, questo uso ha portato all’errata conclusione che il vapore flash sia in qualche modo meno prezioso del cosiddetto vapore vivo.
In qualsiasi sistema a vapore che cerca di massimizzare l’efficienza, il vapore flash sarà separato dal condensato e utilizzato per integrare qualsiasi applicazione di riscaldamento a bassa pressione. Ogni chilogrammo di vapore flash usato in questo modo è un chilogrammo di vapore che non deve essere fornito dalla caldaia. È anche un chilogrammo di vapore che non viene scaricato nell’atmosfera, da dove altrimenti andrebbe perso.
Le ragioni per il recupero del vapore flash sono altrettanto convincenti, sia dal punto di vista economico che ambientale, delle ragioni per il recupero della condensa.
Nota:
La condizione del vapore è determinata da tre variabili:
- Pressione del vapore
- Temperatura del vapore
- Volume del vapore, che dipende dalla pressione e dalla temperatura
La pressione del vapore e la temperatura possono essere misurate relativamente facilmente. Il volume del vapore può avere un riferimento simile.
Costi energetici in aumento
In tempi di costi energetici in aumento, per l’operatore di un sistema di vapore e condensa ad alta intensità energetica è importante capire i processi termodinamici a volte piuttosto sofisticati. Lo stesso sistema di vapore e condensa, che era ancora trattato qualche anno fa in modo piuttosto banale, è ora a causa di prezzi energetici più elevati sono improvvisamente al centro dell’attenzione.
Il modo migliore per identificare i problemi, ha l’operatore. Egli è ogni giorno nella struttura e dovrebbe avere familiarità con ogni valvola e ogni pompa. Le competenze sono spesso sufficienti per controllare il consumo di energia di un impianto e per ottimizzare il senso tecnico.
Le misure di risparmio energetico possono essere attuate già in piccole misure. La prima misura di risparmio energetico, che l’operatore dovrebbe rivedere il suo sistema per determinare se le pompe, valvole di controllo, scambiatori di calore, ecc corrispondono davvero alle condizioni per le quali sono stati originariamente progettati. Questo richiede che l’operatore conosca il suo sistema e capisca le relazioni di base.