Espectroscopia de resonancia magnética nuclear

Frecuencia de resonanciaEditar
Cuando se coloca en un campo magnético, los núcleos activos de RMN (como el 1H o el 13C) absorben la radiación electromagnética a una frecuencia característica del isótopo. La frecuencia de resonancia, la energía de la radiación absorbida y la intensidad de la señal son proporcionales a la intensidad del campo magnético. Por ejemplo, en un campo magnético de 21 Tesla, los núcleos de hidrógeno (comúnmente llamados protones) resuenan a 900 MHz. Es común referirse a un imán de 21 T como un imán de 900 MHz ya que el hidrógeno es el núcleo más común detectado, sin embargo, diferentes núcleos resonarán a diferentes frecuencias en esta intensidad de campo en proporción a sus momentos magnéticos nucleares.
Manejo de la muestraEditar
Un espectrómetro de RMN suele constar de un portamuestras giratorio dentro de un imán muy potente, un emisor de radiofrecuencia y un receptor con una sonda (un conjunto de antena) que va dentro del imán para rodear la muestra, opcionalmente bobinas de gradiente para las mediciones de difusión, y electrónica para controlar el sistema. Por lo general, es necesario hacer girar la muestra para promediar el movimiento difusional; sin embargo, algunos experimentos requieren una muestra estacionaria cuando el movimiento de la solución es una variable importante. Por ejemplo, las mediciones de las constantes de difusión (espectroscopia de difusión ordenada o DOSY) se realizan utilizando una muestra estacionaria con la rotación desactivada, y las celdas de flujo pueden utilizarse para el análisis en línea de los flujos de procesos.
Solventes deuteradosEditar
La gran mayoría de las moléculas de una solución son moléculas de disolvente, y la mayoría de los disolventes habituales son hidrocarburos y, por lo tanto, contienen protones activos de RMN. Para evitar detectar sólo las señales de los átomos de hidrógeno del disolvente, se utilizan disolventes deuterados en los que el 99+% de los protones se sustituyen por deuterio (hidrógeno-2). El disolvente deuterado más utilizado es el deuterocloroformo (CDCl3), aunque pueden utilizarse otros disolventes por diversas razones, como la solubilidad de una muestra, el deseo de controlar el enlace de hidrógeno o los puntos de fusión o ebullición. Los desplazamientos químicos de una molécula cambiarán ligeramente entre los disolventes, y el disolvente utilizado casi siempre se comunicará con los desplazamientos químicos. Los espectros de RMN se calibran a menudo con respecto al pico de protones residuales del disolvente conocido en lugar del tetrametilsilano añadido.
Calce y bloqueoEditar
Para detectar los desplazamientos de frecuencia muy pequeños debidos a la resonancia magnética nuclear, el campo magnético aplicado debe ser constante en todo el volumen de la muestra. Los espectrómetros de RMN de alta resolución utilizan cuñas para ajustar la homogeneidad del campo magnético a partes por billón (ppb) en un volumen de unos pocos centímetros cúbicos. Para detectar y compensar la inhomogeneidad y la deriva del campo magnético, el espectrómetro mantiene un «bloqueo» en la frecuencia del deuterio del disolvente con una unidad de bloqueo separada, que es esencialmente un transmisor adicional y un procesador de RF sintonizados con el núcleo de bloqueo (deuterio) en lugar de los núcleos de la muestra de interés. En los espectrómetros de RMN modernos el calce se ajusta automáticamente, aunque en algunos casos el operador tiene que optimizar los parámetros del calce manualmente para obtener la mejor resolución posible
Adquisición de espectrosEditar
Al excitar la muestra con un pulso de radiofrecuencia (60-1000 MHz), se obtiene una respuesta de resonancia magnética nuclear -un decaimiento de inducción libre (FID)-. Se trata de una señal muy débil, que requiere receptores de radio muy sensibles para ser captada. Se realiza una transformación de Fourier para extraer el espectro en el dominio de la frecuencia a partir de la FID en el dominio del tiempo. El espectro de un solo FID tiene una baja relación señal/ruido, pero mejora fácilmente con el promedio de adquisiciones repetidas. Se pueden adquirir buenos espectros de RMN de 1H con 16 repeticiones, lo que lleva sólo unos minutos. Sin embargo, para los elementos más pesados que el hidrógeno, el tiempo de relajación es bastante largo, por ejemplo, unos 8 segundos para el 13C. Por lo tanto, la adquisición de espectros cuantitativos de elementos pesados puede llevar mucho tiempo, desde decenas de minutos hasta horas.
Después del pulso, los núcleos son, en promedio, excitados a un cierto ángulo frente al campo magnético del espectrómetro. El alcance de la excitación puede controlarse con la anchura del pulso, que suele ser de unos 3-8 µs para el pulso óptimo de 90°. La anchura del pulso puede determinarse trazando la intensidad (con signo) en función de la anchura del pulso. Sigue una curva sinusoidal y, en consecuencia, cambia de signo en las anchuras de pulso correspondientes a los pulsos de 180° y 360°.
Los tiempos de decaimiento de la excitación, medidos típicamente en segundos, dependen de la eficacia de la relajación, que es más rápida para los núcleos más ligeros y en los sólidos, y más lenta para los núcleos más pesados y en las soluciones, y pueden ser muy largos en los gases. Si el segundo pulso de excitación se envía prematuramente antes de que se complete la relajación, el vector de magnetización medio no ha decaído al estado de tierra, lo que afecta a la intensidad de la señal de forma impredecible. En la práctica, las áreas de los picos no son entonces proporcionales a la estequiometría; sólo es posible discernir la presencia, pero no la cantidad de grupos funcionales. Se puede realizar un experimento de recuperación de la inversión para determinar el tiempo de relajación y, por tanto, el retardo necesario entre los pulsos. Se transmite un pulso de 180°, un retardo ajustable y un pulso de 90°. Cuando el pulso de 90° anula exactamente la señal, el retardo corresponde al tiempo necesario para 90° de relajación. La recuperación de la inversión merece la pena para experimentos cuantitativos de 13C, 2D y otros que requieren mucho tiempo.
Desplazamiento químicoEditar
Una carga que gira genera un campo magnético que da lugar a un momento magnético proporcional al giro. En presencia de un campo magnético externo, existen dos estados de espín (para un núcleo de espín 1/2): un espín hacia arriba y un espín hacia abajo, donde uno se alinea con el campo magnético y el otro se opone a él. La diferencia de energía (ΔE) entre los dos estados de espín aumenta a medida que se incrementa la fuerza del campo, pero esta diferencia suele ser muy pequeña, lo que hace que se requieran imanes potentes de RMN (1-20 T para los instrumentos modernos de RMN). La irradiación de la muestra con la energía correspondiente a la separación exacta del estado de espín de un conjunto específico de núcleos provocará la excitación de ese conjunto de núcleos en el estado de energía más bajo al estado de energía más alto.
Para los núcleos de espín 1/2, la diferencia de energía entre los dos estados de espín a una intensidad de campo magnético determinada es proporcional a su momento magnético. Sin embargo, aunque todos los protones tengan los mismos momentos magnéticos, no dan señales de resonancia con los mismos valores de frecuencia. Esta diferencia surge de los diferentes entornos electrónicos del núcleo de interés. Al aplicar un campo magnético externo, estos electrones se mueven en respuesta al campo y generan campos magnéticos locales que se oponen al campo aplicado, mucho más fuerte. Este campo local «blinda» así al protón del campo magnético aplicado, que debe por tanto incrementarse para lograr la resonancia (absorción de la energía rf). Estos incrementos son muy pequeños, normalmente en partes por millón (ppm). Por ejemplo, el pico de protones de un aldehído se desplaza unos 10 ppm en comparación con el pico de un hidrocarburo, ya que, como grupo que retira electrones, el carbonilo desprotege el protón reduciendo la densidad electrónica local. La diferencia entre 2,3487 T y 2,3488 T es, por tanto, de unos 42 ppm. Sin embargo, se suele utilizar una escala de frecuencias para designar las señales de RMN, a pesar de que el espectrómetro puede funcionar barriendo el campo magnético, y así las 42 ppm son 4200 Hz para una frecuencia de referencia (rf) de 100 MHz.
Sin embargo, dado que la localización de las diferentes señales de RMN depende de la intensidad del campo magnético externo y de la frecuencia de referencia, las señales se suelen notificar en relación con una señal de referencia, normalmente la del TMS (tetrametilsilano). Además, como la distribución de las señales de RMN depende del campo, estas frecuencias se dividen por la frecuencia del espectrómetro. Sin embargo, como estamos dividiendo Hz por MHz, el número resultante sería demasiado pequeño, por lo que se multiplica por un millón. Esta operación da, por tanto, un número localizador llamado «desplazamiento químico» con unidades de partes por millón. En general, los desplazamientos químicos de los protones son muy predecibles, ya que los desplazamientos están determinados principalmente por efectos de apantallamiento más simples (densidad de electrones), pero los desplazamientos químicos de muchos núcleos más pesados están más fuertemente influenciados por otros factores, incluyendo los estados excitados (contribución «paramagnética» al tensor de apantallamiento).

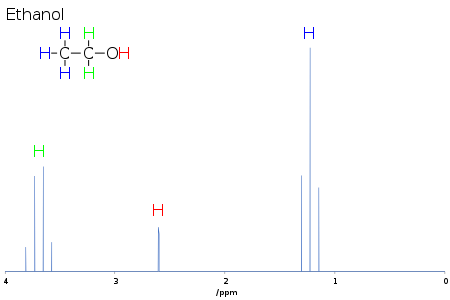
El desplazamiento químico proporciona información sobre la estructura de la molécula. La conversión de los datos brutos en esta información se denomina asignación del espectro. Por ejemplo, para el espectro 1H-NMR del etanol (CH3CH2OH), se esperan señales en cada uno de los tres desplazamientos químicos específicos: uno para el grupo CH3, otro para el grupo CH2 y otro para el grupo OH. Un grupo CH3 típico tiene un desplazamiento de alrededor de 1 ppm, un CH2 unido a un OH tiene un desplazamiento de alrededor de 4 ppm y un OH tiene un desplazamiento de entre 2 y 6 ppm, dependiendo del disolvente utilizado y de la cantidad de enlaces de hidrógeno. Mientras que el átomo de O aleja la densidad de electrones del H unido a través de su enlace sigma mutuo, los pares solitarios de electrones en el O bañan al H en su efecto de blindaje.
En la espectroscopia de RMN paramagnética, las mediciones se realizan en muestras paramagnéticas. El paramagnetismo da lugar a desplazamientos químicos muy diversos. En la espectroscopia de RMN de 1H, el rango de desplazamiento químico puede abarcar hasta miles de ppm.
Debido al movimiento molecular a temperatura ambiente, los tres protones de metilo se promedian durante el experimento de RMN (que suele requerir unos pocos ms). Estos protones se degeneran y forman un pico con el mismo desplazamiento químico.
La forma y el área de los picos también son indicadores de la estructura química. En el ejemplo anterior -el espectro de protones del etanol- el pico CH3 tiene el triple de área que el pico OH. Del mismo modo, el pico CH2 tendría el doble de área que el pico OH, pero sólo 2/3 del área del pico CH3.
El software permite analizar la intensidad de la señal de los picos, que en condiciones de relajación óptima, se correlaciona con el número de protones de ese tipo. El análisis de la intensidad de la señal se realiza por integración, el proceso matemático que calcula el área bajo una curva. El analista debe integrar el pico y no medir su altura porque los picos también tienen anchura y, por tanto, su tamaño depende de su área y no de su altura. Sin embargo, hay que mencionar que el número de protones, o de cualquier otro núcleo observado, sólo es proporcional a la intensidad, o a la integral, de la señal de RMN en los experimentos más simples de RMN unidimensional. En los experimentos más elaborados, por ejemplo, los utilizados habitualmente para obtener espectros de RMN del carbono-13, la integral de las señales depende de la velocidad de relajación del núcleo y de sus constantes de acoplamiento escalar y dipolar. Muy a menudo estos factores son poco conocidos – por lo tanto, la integral de la señal de RMN es muy difícil de interpretar en experimentos de RMN más complicados.
J-couplingEdit
| Multiplicidad | Relación de intensidad | Singlete (s) | 1 |
|---|---|
| Doblete (d) | 1:1 |
| Triplete (t) | 1:2:1 |
| Cuarteto (q) | 1:3:3:1 | Quinteto | 1:4:6:4:1 | Sexteto | 1:5:10:10:5:1 | Septeto | 1:6:15:20:15:6:1 |
Algunas de las informaciones más útiles para la determinación de la estructura en un espectro de RMN unidimensional provienen del acoplamiento J o del acoplamiento escalar (un caso especial de acoplamiento spin-spin) entre los núcleos activos de RMN. Este acoplamiento surge de la interacción de diferentes estados de espín a través de los enlaces químicos de una molécula y da lugar a la división de las señales de RMN. Para un protón, el campo magnético local es ligeramente diferente dependiendo de si un núcleo adyacente apunta hacia o contra el campo magnético del espectrómetro, lo que da lugar a dos señales por protón en lugar de una. Estos patrones de desdoblamiento pueden ser complejos o simples y, del mismo modo, pueden ser directamente interpretables o engañosos. Este acoplamiento proporciona una visión detallada de la conectividad de los átomos en una molécula.
El acoplamiento a n núcleos equivalentes (espín ½) divide la señal en un multiplete n+1 con relaciones de intensidad que siguen el triángulo de Pascal, como se describe a la derecha. El acoplamiento a espines adicionales conducirá a nuevas divisiones de cada componente del multiplete, por ejemplo, el acoplamiento a dos núcleos de espín ½ diferentes con constantes de acoplamiento significativamente diferentes conducirá a un doblete de dobletes (abreviatura: dd). Obsérvese que el acoplamiento entre núcleos que son químicamente equivalentes (es decir, que tienen el mismo desplazamiento químico) no tiene ningún efecto sobre el espectro de RMN y que los acoplamientos entre núcleos que están distantes (normalmente a más de 3 enlaces de distancia para los protones en moléculas flexibles) suelen ser demasiado pequeños para causar desdoblamientos observables. En los compuestos cíclicos y aromáticos pueden observarse con frecuencia acoplamientos de largo alcance en más de tres enlaces, lo que da lugar a patrones de división más complejos.
Por ejemplo, en el espectro de protones del etanol descrito anteriormente, el grupo CH3 se divide en un triplete con una relación de intensidad de 1:2:1 por los dos protones CH2 vecinos. Del mismo modo, el CH2 se divide en un cuarteto con una relación de intensidad de 1:3:3:1 por los tres protones CH3 vecinos. En principio, los dos protones CH2 también se dividirían de nuevo en un doblete para formar un doblete de cuartetos por el protón hidroxilo, pero el intercambio intermolecular del protón hidroxilo ácido a menudo resulta en una pérdida de información de acoplamiento.
El acoplamiento a cualquier núcleo de espín-1/2 como el fósforo-31 o el flúor-19 funciona de esta manera (aunque las magnitudes de las constantes de acoplamiento pueden ser muy diferentes). Pero los patrones de división difieren de los descritos anteriormente para los núcleos con espín mayor que ½ porque el número cuántico de espín tiene más de dos valores posibles. Por ejemplo, el acoplamiento al deuterio (un núcleo de espín 1) divide la señal en un triplete 1:1:1 porque el espín 1 tiene tres estados de espín. Del mismo modo, un núcleo de espín 3/2 como el 35Cl divide la señal en un cuarteto 1:1:1:1 y así sucesivamente.
El acoplamiento combinado con el desplazamiento químico (y la integración para los protones) nos informa no sólo del entorno químico de los núcleos, sino también del número de núcleos activos de RMN vecinos dentro de la molécula. En los espectros más complejos con múltiples picos con desplazamientos químicos similares o en los espectros de núcleos distintos del hidrógeno, el acoplamiento es a menudo la única manera de distinguir los diferentes núcleos.

Acoplamiento de segundo orden (o fuerte)
La descripción anterior supone que la constante de acoplamiento es pequeña en comparación con la diferencia de frecuencias de RMN entre los espines no equivalentes. Si la separación de los desplazamientos disminuye (o la intensidad del acoplamiento aumenta), los patrones de intensidad de los multipletes se distorsionan primero, y luego se vuelven más complejos y menos fáciles de analizar (especialmente si intervienen más de dos espines). La intensificación de algunos picos de un multiplete se consigue a expensas de los restantes, que a veces casi desaparecen en el ruido de fondo, aunque el área integrada bajo los picos permanece constante.En la mayoría de las RMN de alto campo, sin embargo, las distorsiones suelen ser modestas y las distorsiones características (techos) pueden, de hecho, ayudar a identificar los picos relacionados.
Algunos de estos patrones pueden analizarse con el método publicado por John Pople, aunque tiene un alcance limitado.
Los efectos de segundo orden disminuyen a medida que aumenta la diferencia de frecuencia entre los multipletes, de modo que los espectros de RMN de alto campo (es decir, de alta frecuencia) muestran menos distorsión que los espectros de baja frecuencia. Los primeros espectros a 60 MHz eran más propensos a la distorsión que los espectros de máquinas posteriores que suelen operar a frecuencias de 200 MHz o superiores.
Además, como en la figura de la derecha, el acoplamiento J puede utilizarse para identificar la sustitución orto-meta-para de un anillo. El acoplamiento orto es el más fuerte a 15 Hz, le sigue el meta con una media de 2 Hz, y finalmente el acoplamiento para suele ser insignificante para los estudios.
Desigualdad magnéticaEditar
Pueden producirse efectos más sutiles si los espines químicamente equivalentes (es decir, los núcleos relacionados por simetría y que, por tanto, tienen la misma frecuencia de RMN) tienen diferentes relaciones de acoplamiento con los espines externos. Los espines que son químicamente equivalentes pero que no son indistinguibles (basándose en sus relaciones de acoplamiento) se denominan magnéticamente no equivalentes. Por ejemplo, los 4 sitios H del 1,2-diclorobenceno se dividen en dos pares químicamente equivalentes por simetría, pero un miembro individual de uno de los pares tiene diferentes acoplamientos con los espines que forman el otro par. Estos efectos son más comunes en los espectros de RMN de sistemas aromáticos y otros no flexibles, mientras que el promedio conformacional sobre los enlaces C-C en las moléculas flexibles tiende a igualar los acoplamientos entre los protones de los carbonos adyacentes, reduciendo los problemas de la falta de equivalencia magnética.