Spectroscopie par résonance magnétique nucléaire

Fréquence de résonanceEdit
Lorsqu’ils sont placés dans un champ magnétique, les noyaux actifs en RMN (comme le 1H ou le 13C) absorbent le rayonnement électromagnétique à une fréquence caractéristique de l’isotope. La fréquence de résonance, l’énergie du rayonnement absorbé et l’intensité du signal sont proportionnelles à l’intensité du champ magnétique. Par exemple, dans un champ magnétique de 21 Tesla, les noyaux d’hydrogène (communément appelés protons) résonnent à 900 MHz. Il est courant de désigner un aimant de 21 T comme un aimant de 900 MHz car l’hydrogène est le noyau le plus couramment détecté, cependant différents noyaux résonneront à différentes fréquences à cette intensité de champ, proportionnellement à leurs moments magnétiques nucléaires.
Manipulation de l’échantillon
Un spectromètre RMN se compose généralement d’un porte-échantillon tournant à l’intérieur d’un aimant très puissant, d’un émetteur de radiofréquences et d’un récepteur avec une sonde (un ensemble d’antennes) qui va à l’intérieur de l’aimant pour entourer l’échantillon, éventuellement des bobines de gradient pour les mesures de diffusion, et de l’électronique pour contrôler le système. Il est généralement nécessaire de faire tourner l’échantillon pour compenser le mouvement de diffusion, mais certaines expériences nécessitent un échantillon stationnaire lorsque le mouvement de la solution est une variable importante. Par exemple, les mesures des constantes de diffusion (spectroscopie de diffusion ordonnée ou DOSY) se font à l’aide d’un échantillon stationnaire sans rotation, et les cellules à flux peuvent être utilisées pour l’analyse en ligne des flux de processus.
Solvants deutérésEdit
La grande majorité des molécules dans une solution sont des molécules de solvant, et la plupart des solvants réguliers sont des hydrocarbures et contiennent donc des protons actifs en RMN. Pour éviter de détecter uniquement les signaux des atomes d’hydrogène du solvant, on utilise des solvants deutérés où 99+% des protons sont remplacés par du deutérium (hydrogène-2). Le solvant deutéré le plus utilisé est le deutérochloroforme (CDCl3), bien que d’autres solvants puissent être utilisés pour diverses raisons, comme la solubilité d’un échantillon, le désir de contrôler la liaison hydrogène, ou les points de fusion ou d’ébullition. Les déplacements chimiques d’une molécule changent légèrement d’un solvant à l’autre, et le solvant utilisé sera presque toujours signalé avec les déplacements chimiques. Les spectres RMN sont souvent étalonnés par rapport au pic de protons résiduels du solvant connu au lieu du tétraméthylsilane ajouté.
Shim and lockEdit
Pour détecter les très petits décalages de fréquence dus à la résonance magnétique nucléaire, le champ magnétique appliqué doit être constant dans tout le volume de l’échantillon. Les spectromètres RMN haute résolution utilisent des cales pour ajuster l’homogénéité du champ magnétique à des parties par milliard (ppb) dans un volume de quelques centimètres cubes. Afin de détecter et de compenser l’inhomogénéité et la dérive du champ magnétique, le spectromètre maintient un « verrouillage » sur la fréquence du deutérium du solvant à l’aide d’une unité de verrouillage séparée, qui est essentiellement un émetteur et un processeur RF supplémentaires accordés sur le noyau de verrouillage (deutérium) plutôt que sur les noyaux de l’échantillon concerné. Dans les spectromètres RMN modernes, le calage est ajusté automatiquement, bien que dans certains cas, l’opérateur doive optimiser les paramètres du calage manuellement pour obtenir la meilleure résolution possible
Acquisition de spectresEdit
Lors de l’excitation de l’échantillon avec une impulsion de radiofréquence (60-1000 MHz), une réponse de résonance magnétique nucléaire – une désintégration par induction libre (DIF) – est obtenue. C’est un signal très faible, qui nécessite des récepteurs radio sensibles pour être capté. Une transformation de Fourier est effectuée pour extraire le spectre du domaine des fréquences à partir du FID brut du domaine temporel. Le spectre d’un seul FID a un faible rapport signal/bruit, mais il s’améliore facilement avec la moyenne d’acquisitions répétées. De bons spectres de RMN 1H peuvent être acquis avec 16 répétitions, ce qui ne prend que quelques minutes. Cependant, pour les éléments plus lourds que l’hydrogène, le temps de relaxation est plutôt long, par exemple environ 8 secondes pour le 13C. Ainsi, l’acquisition de spectres quantitatifs d’éléments lourds peut être longue, prenant des dizaines de minutes à des heures.
Après l’impulsion, les noyaux sont, en moyenne, excités à un certain angle par rapport au champ magnétique du spectromètre. L’étendue de l’excitation peut être contrôlée avec la largeur de l’impulsion, typiquement environ 3-8 µs pour l’impulsion optimale de 90°. La largeur d’impulsion peut être déterminée en traçant l’intensité (signée) en fonction de la largeur d’impulsion. Elle suit une courbe sinusoïdale et, en conséquence, change de signe aux largeurs d’impulsion correspondant aux impulsions de 180° et 360°.
Les temps de décroissance de l’excitation, généralement mesurés en secondes, dépendent de l’efficacité de la relaxation, qui est plus rapide pour les noyaux légers et dans les solides, et plus lente pour les noyaux plus lourds et dans les solutions, et ils peuvent être très longs dans les gaz. Si la deuxième impulsion d’excitation est envoyée prématurément avant que la relaxation ne soit complète, le vecteur d’aimantation moyen n’a pas décru jusqu’à l’état fondamental, ce qui affecte l’intensité du signal de manière imprévisible. En pratique, les surfaces des pics ne sont alors pas proportionnelles à la stœchiométrie ; on ne peut discerner que la présence, mais pas la quantité, de groupes fonctionnels. Une expérience d’inversion-récupération peut être réalisée pour déterminer le temps de relaxation et donc le délai nécessaire entre les impulsions. On transmet une impulsion de 180°, un délai réglable et une impulsion de 90°. Lorsque l’impulsion à 90° annule exactement le signal, le délai correspond au temps nécessaire pour 90° de relaxation. La récupération de l’inversion est intéressante pour les expériences de quantification du 13C, de la 2D et d’autres expériences qui prennent beaucoup de temps.
Modification du déplacement chimique
Une charge en rotation génère un champ magnétique qui se traduit par un moment magnétique proportionnel au spin. En présence d’un champ magnétique externe, deux états de spin existent (pour un noyau de spin 1/2) : un spin up et un spin down, où l’un s’aligne avec le champ magnétique et l’autre s’y oppose. La différence d’énergie (ΔE) entre les deux états de spin augmente avec l’intensité du champ, mais cette différence est généralement très faible, d’où la nécessité de disposer d’aimants RMN puissants (1-20 T pour les instruments RMN modernes). L’irradiation de l’échantillon avec une énergie correspondant à la séparation exacte des états de spin d’un ensemble spécifique de noyaux provoquera l’excitation de cet ensemble de noyaux dans l’état d’énergie inférieur vers l’état d’énergie supérieur.
Pour les noyaux de spin 1/2, la différence d’énergie entre les deux états de spin à une intensité de champ magnétique donnée est proportionnelle à leur moment magnétique. Cependant, même si tous les protons ont les mêmes moments magnétiques, ils ne donnent pas de signaux de résonance aux mêmes valeurs de fréquence. Cette différence provient des différents environnements électroniques du noyau concerné. Lors de l’application d’un champ magnétique externe, ces électrons se déplacent en réponse au champ et génèrent des champs magnétiques locaux qui s’opposent au champ appliqué, beaucoup plus fort. Ce champ local « protège » ainsi le proton du champ magnétique appliqué, qui doit donc être augmenté pour atteindre la résonance (absorption de l’énergie RF). Ces augmentations sont très faibles, généralement en parties par million (ppm). Par exemple, le pic de proton d’un aldéhyde est décalé d’environ 10 ppm par rapport au pic d’un hydrocarbure, car en tant que groupe attracteur d’électrons, le carbonyle désamorce le proton en réduisant la densité électronique locale. La différence entre 2,3487 T et 2,3488 T est donc d’environ 42 ppm. Cependant une échelle de fréquence est couramment utilisée pour désigner les signaux RMN, même si le spectromètre peut fonctionner par balayage du champ magnétique, et ainsi les 42 ppm correspondent à 4200 Hz pour une fréquence de référence (rf) de 100 MHz.
Cependant, étant donné que la localisation des différents signaux RMN dépend de l’intensité du champ magnétique externe et de la fréquence de référence, les signaux sont généralement rapportés par rapport à un signal de référence, habituellement celui du TMS (tétraméthylsilane). De plus, comme la distribution des signaux RMN dépend du champ, ces fréquences sont divisées par la fréquence du spectromètre. Cependant, comme nous divisons les Hz par les MHz, le nombre résultant serait trop petit, et il est donc multiplié par un million. Cette opération donne donc un nombre de repérage appelé « déplacement chimique » avec des unités de parties par million. En général, les déplacements chimiques des protons sont très prévisibles car ils sont principalement déterminés par des effets de blindage plus simples (densité électronique), mais les déplacements chimiques de nombreux noyaux plus lourds sont plus fortement influencés par d’autres facteurs, notamment les états excités (contribution « paramagnétique » au tenseur de blindage).

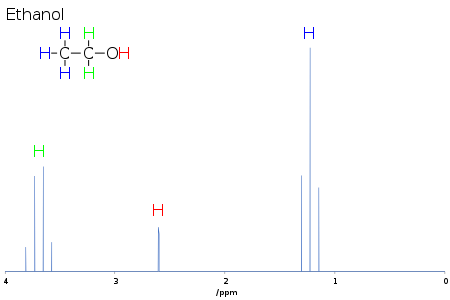
Le déplacement chimique fournit des informations sur la structure de la molécule. La conversion des données brutes en ces informations s’appelle l’attribution du spectre. Par exemple, pour le spectre 1H-RMN de l’éthanol (CH3CH2OH), on s’attendrait à des signaux à chacun de trois déplacements chimiques spécifiques : un pour le groupe CH3, un pour le groupe CH2 et un pour le groupe OH. Un groupe CH3 typique a un décalage d’environ 1 ppm, un CH2 attaché à un OH a un décalage d’environ 4 ppm et un OH a un décalage de 2 à 6 ppm selon le solvant utilisé et le degré de liaison hydrogène. Alors que l’atome O attire effectivement la densité électronique loin de l’H attaché par leur liaison sigma mutuelle, les paires d’électrons solitaires sur l’O baignent l’H dans leur effet de blindage.
Dans la spectroscopie RMN paramagnétique, les mesures sont effectuées sur des échantillons paramagnétiques. Le paramagnétisme donne lieu à des déplacements chimiques très divers. En spectroscopie RMN 1H, la plage de déplacement chimique peut s’étendre jusqu’à des milliers de ppm.
En raison du mouvement moléculaire à température ambiante, les trois protons méthyles s’équilibrent pendant l’expérience RMN (qui nécessite généralement quelques ms). Ces protons deviennent dégénérés et forment un pic au même déplacement chimique.
La forme et la surface des pics sont également des indicateurs de la structure chimique. Dans l’exemple ci-dessus – le spectre protonique de l’éthanol – le pic CH3 a une surface trois fois supérieure à celle du pic OH. De même, le pic CH2 aurait deux fois l’aire du pic OH mais seulement 2/3 de l’aire du pic CH3.
Un logiciel permet d’analyser l’intensité du signal des pics, qui dans des conditions de relaxation optimale, sont corrélés avec le nombre de protons de ce type. L’analyse de l’intensité du signal se fait par intégration – le processus mathématique qui calcule l’aire sous une courbe. L’analyste doit intégrer le pic et non pas mesurer sa hauteur car les pics ont aussi une largeur – et donc sa taille dépend de sa surface et non de sa hauteur. Il convient toutefois de mentionner que le nombre de protons, ou de tout autre noyau observé, n’est proportionnel à l’intensité, ou à l’intégrale, du signal RMN que dans les expériences RMN unidimensionnelles les plus simples. Dans les expériences plus élaborées, par exemple celles qui sont généralement utilisées pour obtenir des spectres RMN du carbone 13, l’intégrale des signaux dépend de la vitesse de relaxation du noyau et de ses constantes de couplage scalaire et dipolaire. Très souvent, ces facteurs sont mal connus – par conséquent, l’intégrale du signal RMN est très difficile à interpréter dans les expériences RMN plus compliquées.
J-couplingEdit
| Multiplicité | Rapport d’intensité |
|---|---|
| Singlet (s) | 1 | Doublet (d) | 1 :1 | Triplet (t) | 1:2:1 | Quartet (q) | 1:3:3:1 | Quintet | 1 :4:6:4:1 | Sextet | 1:5:10:10:5:1 | Septet | 1:6:15:20:15:6 :1 |
Certaines des informations les plus utiles pour la détermination de la structure dans un spectre RMN unidimensionnel proviennent du couplage J ou du couplage scalaire (un cas particulier de couplage spin-spin) entre les noyaux actifs en RMN. Ce couplage résulte de l’interaction de différents états de spin à travers les liaisons chimiques d’une molécule et entraîne le fractionnement des signaux RMN. Pour un proton, le champ magnétique local est légèrement différent selon qu’un noyau adjacent pointe vers ou contre le champ magnétique du spectromètre, ce qui donne lieu à deux signaux par proton au lieu d’un. Ces schémas de fractionnement peuvent être complexes ou simples et, de même, ils peuvent être directement interprétables ou trompeurs. Ce couplage fournit un aperçu détaillé de la connectivité des atomes dans une molécule.
Le couplage à n noyaux équivalents (spin ½) divise le signal en un multiplet n+1 avec des rapports d’intensité suivant le triangle de Pascal, comme décrit à droite. Le couplage à des spins supplémentaires entraînera d’autres divisions de chaque composante du multiplet, par exemple, le couplage à deux noyaux de spin ½ différents avec des constantes de couplage significativement différentes conduira à un doublet de doublets (abréviation : dd). Notez que le couplage entre des noyaux chimiquement équivalents (c’est-à-dire ayant le même déplacement chimique) n’a aucun effet sur les spectres RMN et que les couplages entre noyaux distants (généralement plus de 3 liaisons entre eux pour les protons dans les molécules flexibles) sont généralement trop faibles pour provoquer des fractionnements observables. Des couplages à longue distance sur plus de trois liaisons peuvent souvent être observés dans les composés cycliques et aromatiques, ce qui entraîne des schémas de fractionnement plus complexes.
Par exemple, dans le spectre protonique de l’éthanol décrit ci-dessus, le groupe CH3 est fractionné en un triplet avec un rapport d’intensité de 1:2:1 par les deux protons CH2 voisins. De même, le groupe CH2 est divisé en un quartet avec un rapport d’intensité de 1:3:3:1 par les trois protons CH3 voisins. En principe, les deux protons CH2 seraient également scindés à nouveau en un doublet pour former un doublet de quatuors par le proton hydroxyle, mais l’échange intermoléculaire du proton hydroxyle acide entraîne souvent une perte d’information sur le couplage.
Le couplage à n’importe quel noyau de spin-1/2 tel que le phosphore-31 ou le fluor-19 fonctionne de cette manière (bien que les amplitudes des constantes de couplage puissent être très différentes). Mais les schémas de fractionnement diffèrent de ceux décrits ci-dessus pour les noyaux dont le spin est supérieur à ½, car le nombre quantique de spin a plus de deux valeurs possibles. Par exemple, le couplage au deutérium (un noyau de spin 1) divise le signal en un triplet 1:1:1 car le spin 1 possède trois états de spin. De même, un noyau de spin 3/2 tel que 35Cl divise un signal en un quartet 1:1:1:1 et ainsi de suite.
Le couplage combiné au déplacement chimique (et à l’intégration pour les protons) nous renseigne non seulement sur l’environnement chimique des noyaux, mais aussi sur le nombre de noyaux voisins actifs en RMN au sein de la molécule. Dans les spectres plus complexes avec plusieurs pics à des déplacements chimiques similaires ou dans les spectres de noyaux autres que l’hydrogène, le couplage est souvent le seul moyen de distinguer les différents noyaux.

Couplage de second ordre (ou fort)Modifié
La description ci-dessus suppose que la constante de couplage est faible par rapport à la différence de fréquences RMN entre les spins non équivalents. Si la séparation des déplacements diminue (ou si la force de couplage augmente), les modèles d’intensité des multiplets sont d’abord déformés, puis deviennent plus complexes et moins faciles à analyser (surtout si plus de deux spins sont impliqués). L’intensification de certains pics d’un multiplet se fait au détriment des autres, qui disparaissent parfois presque dans le bruit de fond, bien que l’aire intégrée sous les pics reste constante.Dans la plupart des RMN à haut champ, cependant, les distorsions sont généralement modestes et les distorsions caractéristiques (toit) peuvent en fait aider à identifier les pics apparentés.
Certains de ces motifs peuvent être analysés avec la méthode publiée par John Pople, bien qu’elle ait une portée limitée.
Les effets de second ordre diminuent à mesure que la différence de fréquence entre les multiplets augmente, de sorte que les spectres RMN à haut champ (c’est-à-dire à haute fréquence) présentent moins de distorsion que les spectres à plus basse fréquence. Les premiers spectres à 60 MHz étaient plus sujets à la distorsion que les spectres des machines ultérieures fonctionnant généralement à des fréquences de 200 MHz ou plus.
En outre, comme dans la figure de droite, le couplage J peut être utilisé pour identifier la substitution ortho-méta-para d’un cycle. Le couplage ortho est le plus fort à 15 Hz, le méta suit avec une moyenne de 2 Hz, et enfin le couplage para est généralement insignifiant pour les études.
Magnetic inequivalenceEdit
Des effets plus subtils peuvent se produire si des spins chimiquement équivalents (c’est-à-dire des noyaux reliés par symétrie et ayant donc la même fréquence RMN) ont des relations de couplage différentes avec les spins externes. Par exemple, les sites 4 H du 1,2-dichlorobenzène se divisent en deux paires chimiquement équivalentes par symétrie, mais un membre individuel de l’une des paires a des couplages différents avec les spins qui composent l’autre paire.L’inégalité magnétique peut conduire à des spectres très complexes qui ne peuvent être analysés que par modélisation informatique. De tels effets sont plus courants dans les spectres RMN des systèmes aromatiques et d’autres systèmes non flexibles, tandis que la moyenne conformationnelle autour des liaisons C-C dans les molécules flexibles tend à égaliser les couplages entre les protons sur les carbones adjacents, ce qui réduit les problèmes d’inéquivalence magnétique.