Perché i metalli conducono così bene il calore e l’elettricità? Quali metalli conducono meglio?
Struttura dei metalli
Le strutture dei metalli puri sono semplici da descrivere poiché gli atomi che formano questi metalli possono essere pensati come sfere perfette identiche. Più specificamente la struttura metallica consiste di “ioni positivi allineati” (cationi) in un “mare” di elettroni delocalizzati. Questo significa che gli elettroni sono liberi di muoversi in tutta la struttura, e dà origine a proprietà come la conduttività.
Quali sono i diversi tipi di legame?
Legami covalenti
Un legame covalente è un legame che si forma quando due atomi condividono elettroni. Esempi di composti con legami covalenti sono l’acqua, lo zucchero e l’anidride carbonica.
Legami ionici
Il legame ionico è il trasferimento completo di elettroni di valenza tra un metallo e un non-metallo. Questo si traduce in due ioni di carica opposta che si attraggono a vicenda. Nei legami ionici, il metallo perde elettroni per diventare un catione con carica positiva, mentre il non metallo accetta quegli elettroni per diventare un anione con carica negativa. Un esempio di legame ionico sarebbe il sale (NaCl).
Legami metallici
Il legame metallico è il risultato della forza di attrazione elettrostatica che si verifica tra gli elettroni di conduzione (sotto forma di una nuvola elettronica di elettroni delocalizzati) e gli ioni metallici con carica positiva. Può essere descritto come la condivisione di elettroni liberi tra un reticolo di ioni caricati positivamente (cationi). Il legame metallico spiega molte proprietà fisiche dei metalli, come la forza, la duttilità, la resistività e la conducibilità termica ed elettrica, l’opacità e la lucentezza.
Elettroni mobili delocalizzati nei metalli —
È il movimento libero degli elettroni nei metalli che dà loro la conducibilità.
Conducibilità elettrica
I metalli contengono elettroni delocalizzati in libero movimento. Quando viene applicata una tensione elettrica, un campo elettrico all’interno del metallo innesca il movimento degli elettroni, facendoli spostare da un’estremità all’altra del conduttore. Gli elettroni si muoveranno verso il lato positivo.
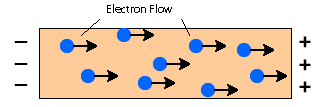
Conduzione del calore
Il metallo è una buona conduzione del calore. La conduzione avviene quando una sostanza viene riscaldata, le particelle guadagnano più energia e vibrano di più. Queste molecole poi si scontrano con le particelle vicine e trasferiscono loro parte della loro energia. Questo poi continua e passa l’energia dall’estremità calda all’estremità più fredda della sostanza.
Perché i metalli conducono così bene il calore?
Gli elettroni nei metalli sono elettroni delocalizzati e sono elettroni liberi di muoversi, quindi quando guadagnano energia (calore) vibrano più rapidamente e possono muoversi, il che significa che possono trasmettere l’energia più rapidamente.
Quali metalli conducono meglio?
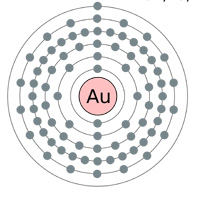
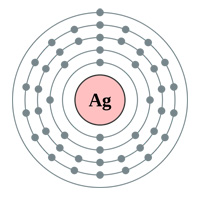
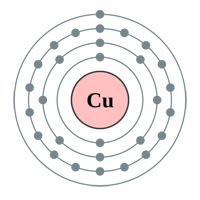
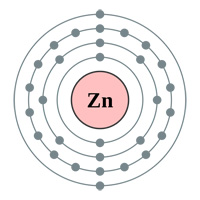
Sopra: Gusci di elettroni Oro (au), Argento (Ag), Rame (Cu) e Zinco (Zn). La logica farebbe pensare che l’oro sia il miglior conduttore avendo un solo elettrone dell’orbitale s nell’ultimo guscio (grafico sopra) … allora perché l’argento e il rame sono effettivamente migliori (vedi tabella sotto).
|
Conduttività dei metalli
|
>S/m
|
|
| Argento | 6.30×10 7 | |
| Rame | 5.96×10 7 | |
| Oro | 4.10×10 7 | |
| Alluminio | 3.50×10 7 | |
| Zinco | 1.69×10 7 |
L’argento ha un raggio atomico maggiore (160 pm) dell’oro (135 pm), nonostante il fatto che l’oro abbia più elettroni dell’argento! Per una ragione di questo, vedi il commento qui sotto.
Nota: L’argento è un conduttore migliore dell’oro, ma l’oro è più desiderabile perché non si corrode. (Il rame è il più comune perché è il più conveniente) La risposta è un po’ complicata e mettiamo qui una delle migliori risposte che abbiamo visto per chi ha familiarità con il materiale.
“L’argento si trova nel mezzo dei metalli di transizione circa a metà strada tra i gas nobili e i metalli alcalini. Nella colonna 11 della tavola periodica, tutti questi elementi (rame, argento e oro) hanno un singolo elettrone dell’orbitale s nel guscio esterno (anche il platino, nella colonna 10).
La struttura orbitale degli elettroni di questi elementi non ha una particolare affinità per guadagnare un elettrone o perdere un elettrone verso i gas nobili che sono più pesanti o più leggeri, perché stanno a metà strada nel mezzo. In generale questo significa che non ci vuole molta energia per togliere temporaneamente un elettrone o aggiungerne uno temporaneamente. Le affinità elettroniche specifiche e i potenziali di ionizzazione sono diversi, e per quanto riguarda la conduzione, avere energie relativamente basse per questi due criteri è piuttosto importante.
Se questi fossero gli unici criteri, l’oro sarebbe un conduttore migliore dell’argento, ma l’oro ha 14 elettroni f in più sotto i 10 elettroni d-orbitali e il singolo elettrone s-orbitale. I 14 elettroni f sono dovuti agli atomi extra nella serie degli attinidi. Con 14 elettroni extra che apparentemente spingono fuori gli elettroni d ed s, si potrebbe pensare che l’elettrone s sia semplicemente seduto là fuori “maturo” per la conduzione (quasi nessuna energia è necessaria per farlo fuori), ma NOOO. Gli elettroni dell’orbitale f sono impacchettati in modo tale da rendere il raggio atomico dell’oro effettivamente più piccolo di quello dell’argento – non di molto, ma è più piccolo. Un raggio più piccolo significa più forza dal nucleo sugli elettroni esterni, quindi l’argento vince nella “gara” di conduttività. Ricorda, la forza dovuta alla carica elettrica è inversamente proporzionale al quadrato della distanza. Più due cariche sono vicine, maggiore è la forza tra loro.
Sia il rame che il platino hanno diametri ancora più piccoli; quindi più forza dal nucleo, quindi più energia per staccare l’elettrone s solitario, quindi conduttività inferiore.
Altri elementi con un singolo elettrone dell’orbitale s seduto là fuori “maturo per l’arrivo del raccoglitore di conduzione”, hanno anche raggi atomici più bassi (molibdeno, niobio, cromo, rutenio, rodio) dell’argento.
Così, è principalmente dove si trova – dove ‘madre natura’ ha messo l’argento nella tavola periodica, che detta la sua eccellente conduttività.”
Fonte da tlbs101 Yahoo