Drug-Induced Hypertension
US Pharm. 2008;33(9):HS11-HS20.
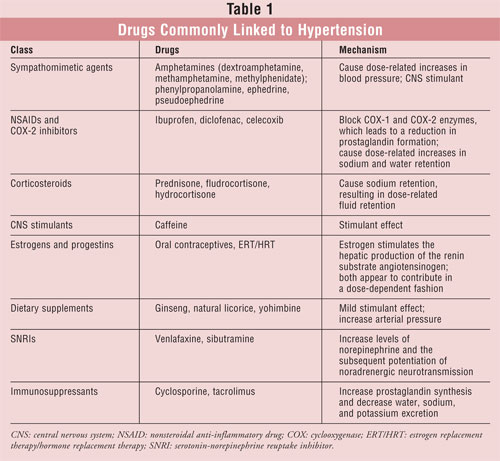
Pharmaceuten krijgen vaak vragen over de effecten van geneesmiddelen op de bloeddruk. Zo bestaat er nog steeds bezorgdheid over vrij verkrijgbare hoest- en verkoudheidsproducten, ook al zijn sommige ingrediënten, zoals fenylpropanolamine, uit de Amerikaanse markt genomen. Hoewel slechts enkele klassen van geneesmiddelen klinisch significante stijgingen van de bloeddruk veroorzaken, moeten apothekers op de hoogte zijn van geneesmiddelen die een effectieve bloeddrukbeheersing kunnen belemmeren. Een overzicht van interacties tussen geneesmiddelen en antihypertensiva valt buiten het bestek van dit artikel. Wel zullen enkele van de meest voorkomende voorbeelden van door geneesmiddelen veroorzaakte hypertensie worden besproken (TABEL 1). Door geneesmiddelen veroorzaakte bloeddrukverhogingen vormen een belangrijke en modificeerbare oorzaak van secundaire hypertensie; het is daarom van groot belang dat apothekers deze causale relatie onderkennen.
Sympathomimetische middelen
Het is algemeen bekend dat sympathomimetische aminen dosisgerelateerde bloeddrukverhogingen veroorzaken.1-4 Hoewel door sympathomimetica veroorzaakte hypertensie bij gezonde patiënten klinisch niet significant is, kan het bij anderen gevaarlijk worden.1-4 Sympathomimetische aminen omvatten amfetaminen en vergelijkbare verbindingen, zoals pseudo-efedrine, fenylpropanolamine, en efedrine. Vroeger zaten deze verbindingen in sommige OTC-preparaten voor hoest en verkoudheid. Omdat het gebruik van fenylpropanolamine in verband werd gebracht met hoge bloeddruk en beroertes, heeft de FDA het in november 2000 van de markt gehaald.3,4
Pseudoefedrine: Pseudo-efedrine is een bronchodilatator en nasale vasoconstrictor die over het algemeen onschadelijk is wanneer het in aanbevolen doses wordt gebruikt. Omdat het echter misbruikt kan worden, is het in veel winkels alleen achter de toonbank te koop. Pseudo-efedrine wordt algemeen gebruikt om de symptomen van rinitis en rinorroe te behandelen, maar de effecten op de bloeddruk en de hartslag blijven onzeker. Vanwege de farmacologische gelijkenis met efedrine en fenylpropanolamine wordt het gebruik van pseudo-efedrine ook vermeden bij patiënten met hoge bloeddruk.
Salerno e.a. hebben onderzocht of pseudo-efedrine klinisch zinvolle bloeddruk- en hartslagverhogingen veroorzaakt.5 In deze meta-analyse waren de primaire gegevens de systolische en diastolische bloeddruk en de hartslag. Vierentwintig klinische trials hadden informatie over vitale functies en includeerden in totaal 1.285 patiënten. Deze analyse toonde aan dat pseudo-efedrine een kleine gemiddelde stijging van de systolische bloeddruk veroorzaakt (ongeveer 1 mmHg), zonder significant effect op de diastolische bloeddruk, en een lichte stijging van de hartslag (ongeveer 3 slagen per minuut). Onmiddellijk vrijkomende formuleringen hadden een groter effect dan formuleringen met langdurige afgifte, hetgeen op basis van de farmacokinetiek te verwachten zou zijn. Bij de formuleringen met onmiddellijke afgifte was er een dosisgerelateerde toename in alle drie cardiovasculaire variabelen. Sterkere stijgingen in zowel systolische als diastolische bloeddruk werden waargenomen met toenemende doses pseudo-efedrine. Vrouwen leken iets minder gevoelig te zijn voor de cardiovasculaire effecten dan mannen. Bij patiënten bij wie de hypertensie stabiel en onder controle was, verhoogde pseudo-efedrine therapie de systolische bloeddruk, maar had geen effect op de diastolische druk. Er was geen effect op de hartslag bij behandelde hypertensieve patiënten, hoewel dit kan komen doordat veel patiënten bètablokkers kregen. Er was geen documentatie van klinisch significante nadelige uitkomsten, zoals hypertensieve noodgevallen, beroerte of hartritmestoornissen. Andere onderzoekers hebben op vergelijkbare wijze geconcludeerd dat pseudoefedrine bij gebruik in standaarddoses geen klinisch significant effect heeft op de systolische of diastolische bloeddruk bij patiënten met gecontroleerde hypertensie.6
Pharmaceuten moeten patiënten erop wijzen dat pseudoefedrine de bloeddruk en de hartslag in bescheiden mate kan verhogen. Deze effecten zijn het grootst bij immediate-release formuleringen, hogere doses en kortdurende medicatietoediening. Patiënten met een stabiele, gecontroleerde hypertensie lijken geen hoger risico op bloeddrukverhoging te lopen dan patiënten zonder hypertensie. Men kan echter niet voorspellen hoe een individuele patiënt zal reageren. De risico-batenverhouding moet zorgvuldig worden geëvalueerd alvorens een sympathomimetisch middel te gebruiken bij personen met hypertensie. Apothekers moeten patiënten met hart- en vaatziekten instrueren om hun bloeddruk zorgvuldig te controleren na het starten met pseudo-efedrine bevattende medicatie. Producten met verlengde afgifte hebben over het algemeen de voorkeur om bloeddrukverhoging te voorkomen. Als alternatief kunnen intranasale decongestiva zoals oxymetazoline worden gebruikt, omdat van deze middelen niet is aangetoond dat ze hypertensie veroorzaken wanneer ze in de aanbevolen doses worden gebruikt.7
Amphetaminederivaten: Een verscheidenheid aan geneesmiddelen die worden gebruikt voor narcolepsie en aandachtstekortstoornis/hyperactiviteitstoornis zijn chemisch verwant aan amfetamine. Deze stimulerende middelen voor het centrale zenuwstelsel (CZS) omvatten dextroamfetamine, methamfetamine en methylfenidaat. De FDA heeft onlangs een waarschuwing afgegeven voor dextroamfetamine, waarin staat dat het gebruik van CNS-stimulantia in de gebruikelijke doses bij kinderen en adolescenten met ernstige hartproblemen en structurele hartafwijkingen in verband is gebracht met plotseling overlijden.8 Nadelige cardiovasculaire voorvallen die worden veroorzaakt door stimulantia zijn echter niet beperkt tot kinderen. Volwassenen met bekende hartaandoeningen hebben ook een verhoogd risico op plotseling overlijden laten zien bij gebruik van stimulantia in normale doses. Als algemene regel geldt dat amfetamine-gerelateerde verbindingen (d.w.z. CNS-stimulantia) dienen te worden vermeden bij patiënten met bekende ernstige structurele hartafwijkingen, cardiomyopathie, ernstige hartritmeafwijkingen, of andere ernstige hartproblemen die het risico op plotseling overlijden verhogen. Stijgingen van zowel de hartslag als de bloeddruk zijn waargenomen bij kinderen die geneesmiddelen uit deze klasse kregen.9 Dit potentiële cardiovasculaire risico moet dus worden afgewogen tegen de gunstige gedragseffecten van deze geneesmiddelen.
NSAID’s en COX-2-remmers
Nonsteroïde anti-inflammatoire geneesmiddelen (NSAID’s) hebben mogelijk nadelige effecten op de bloeddruk.10,11 NSAID’s blokkeren zowel de cyclo-oxygenase-1 (COX-1) als de COX-2 enzymen, wat leidt tot een vermindering van de prostaglandinevorming. Deze geneesmiddelen kunnen op grote schaal gunstige en schadelijke effecten hebben, afhankelijk van de context van de patiënt. De door NSAID’s veroorzaakte verhoogde bloeddruk is te wijten aan de renale effecten van deze geneesmiddelen. NSAID’s veroorzaken een dosis-gerelateerde toename van natrium- en waterretentie. Dit effect wordt ook gezien bij COX-2 selectieve middelen, zoals celecoxib.11 De COX-1 en COX-2 isovormen komen beide tot expressie in de normale volwassen nier, waarbij COX-1 in de glomerulus en afferente arteriole en COX-2 in de afferente arteriole, de podocyten en de macula densa.12 De specifieke locatie van elk van deze isoenzymen in de nier vertaalt zich in opmerkelijk verschillende effecten op de nierfunctie. De prostaglandinen die door COX-1 worden geproduceerd, beïnvloeden voornamelijk de renale homeostase door vaatverwijding in het renale vaatbed te bevorderen, de renale vaatweerstand te verlagen en bijgevolg de nierperfusie te verhogen. Prostaglandinen geproduceerd door het COX-2 iso-enzym hebben diuretische en natriuretische effecten.12,13 Bij patiënten die hemodynamisch gecompromitteerd zijn, zijn de effecten van de twee iso-enzymen essentieel voor het behoud van de nierperfusie vanwege hun vaatverwijdende effecten. Omdat NSAID’s de productie van de prostaglandines COX-1 en COX-2 blokkeren, zijn nierbijwerkingen niet ongewoon, en komen voor bij ongeveer 1% tot 5% van de NSAID-gebruikers.13
Door het natriuretische effect van COX-2 te remmen, waardoor de natriumretentie toeneemt, brengen alle NSAID’s het daaruit voortvloeiende risico van verhoogde vochtretentie met zich mee.14 Daarnaast kan de remming van vaatverwijdende prostaglandines en de productie van vaatvernauwende factoren, namelijk endotheline-1, bijdragen aan de inductie van hypertensie bij een normotensieve en/of gecontroleerde hypertensieve patiënt.14
In een vergelijking van celecoxib met diclofenac, uitgevoerd bij 287 patiënten met artritis, werden cardiovasculaire en renale bijwerkingen gezien bij 79 patiënten (27,8%), waarbij hypertensie het meest voorkwam (16,6%).14 Er was geen statistisch verschil in de incidentie van hypertensie tussen de traditionele NSAID en COX-2 groepen. Deze initiatie van hypertensie door NSAID’s is vooral belangrijk in de discussie over de veiligheid van COX-2 in het licht van het feit dat de hypertensieve status een belangrijke risicofactor is voor de progressie van vrijwel alle cardiovasculaire ziekten, waaronder beroertes, myocardinfarct en congestief hartfalen.15
Een recente meta-analyse van COX-2 remmers en hun effecten op de bloeddruk werd gepubliceerd.16 Er werden gegevens verzameld bij 45.451 patiënten uit 19 klinische onderzoeken. Interessant genoeg bleek er een iets grotere bloeddrukverhoging te zijn met COX-2-remmers in vergelijking met placebo en niet-selectieve NSAID’s (bijv. ibuprofen en diclofenac). Rofecoxib leek een groter risico te geven op het ontwikkelen van klinisch belangrijke verhogingen van zowel de systolische als de diastolische bloeddruk in vergelijking met celecoxib. Rofecoxib werd echter in 2004 vrijwillig van de markt gehaald vanwege bezorgdheid over een verhoogd risico op hartaanvallen en beroertes.17
Omwille van de wijdverbreide beschikbaarheid van NSAID’s zonder voorschrift, lopen veel patiënten met hypertensie het risico op verergering van de bloeddrukeffecten veroorzaakt door deze geneesmiddelen. Apothekers moeten een zorgvuldige medicatieanamnese afnemen en specifiek informeren naar het vrij verkrijgbare gebruik van NSAID’s. Patiënten met hypertensie moeten nauwlettender worden gecontroleerd op bloeddrukverhogingen bij gebruik van NSAID’s. Patiënten moeten erop worden gewezen dat deze bijwerking meestal dosisgerelateerd is, maar niet altijd voorspelbaar is. Het nadelige effect van alle NSAID’s en COX-2 remmers op de bloeddruk heeft mogelijk de meeste klinische betekenis bij ouderen, bij wie de prevalentie van artritis, hypertensie en NSAID-gebruik hoog is.18
Corticosteroïden
Alle corticosteroïden, inclusief prednison, kunnen natriumretentie veroorzaken, met dosisgerelateerde vochtretentie tot gevolg.19 Corticosteroïden met een sterke mineralocorticoïde werking, zoals fludrocortison en hydrocortison, veroorzaken de grootste hoeveelheid vochtretentie. Sommige corticosteroïden die geen significante mineralocorticoïde werking hebben (bijv. dexamethason, triamcinolon, betamethason), kunnen echter geringe vochtretentie veroorzaken.20 Corticosteroïd-geïnduceerde vochtretentie kan ernstig genoeg zijn om hypertensie te veroorzaken, en patiënten met reeds bestaande hypertensie kunnen een verslechtering van de bloeddrukcontrole ontwikkelen wanneer deze geneesmiddelen worden gestart. Het belangrijkste mechanisme van door corticosteroïden veroorzaakte hypertensie is de overstimulatie van de mineralocorticoïdreceptor, wat leidt tot natriumretentie in de nieren. Dit resulteert in volume-expansie en een daaropvolgende stijging van de bloeddruk. Corticosteroïd-geïnduceerde hypertensie kan reageren op behandeling met diuretica.21 De kleinste effectieve dosis en de kortste duur van de steroïdtherapie moeten worden gebruikt om de ontwikkeling van deze bijwerking te verminderen.
Fludrocortison veroorzaakt aanzienlijke bloeddrukverhogingen en is daarom nuttig bij de behandeling van patiënten met posturale hypotensie. In een studie met 64 oudere patiënten die gedurende ongeveer vijf maanden een gemiddelde dosis van 75 mcg fludrocortison kregen, moesten vier patiënten zich terugtrekken vanwege door het middel veroorzaakte hypertensie.22 De onderzoekers van de studie concludeerden dat fludrocortison slecht werd verdragen bij oudere patiënten, zelfs bij lage doses.
Cafeïne
De effecten van cafeïne op de bloeddrukcontrole zijn niet goed gedefinieerd. Onlangs werd een meta-analyse gepubliceerd van gerandomiseerde gecontroleerde onderzoeken waarin het effect van koffie of cafeïne alleen op het bloeddrukniveau werd geanalyseerd.23 In totaal werden 16 onderzoeken met gerandomiseerde, gecontroleerde ontwerpen geselecteerd voor beoordeling, die 1.010 proefpersonen vertegenwoordigden. Na samenvoeging van deze onderzoeken werd een stijging van 2,04 mmHg in systolische bloeddruk en van 0,73 mmHg in diastolische bloeddruk gevonden. Wanneer de koffie- en cafeïneproeven afzonderlijk werden geanalyseerd, waren de bloeddrukstijgingen groter bij cafeïne (410 mg/dag) dan bij koffie (725 ml/dag). De effecten van koffie en cafeïne op de hartslag waren niet significant.
Estrogenen en Progestins
Chronisch gebruik van orale anticonceptiva kan bij bepaalde vrouwen de bloeddruk licht verhogen en kan andere nadelige effecten hebben op het cardiovasculaire risico. In vroege epidemiologische studies waarbij oestrogeen in hoge doses werd gebruikt, werden gemiddelde bloeddrukverhogingen gevonden van 3 tot 6 mmHg systolisch en 2 tot 5 mmHg diastolisch, waarbij ongeveer 5% van de vrouwen nieuwe hypertensie ontwikkelde.24 De kans hierop was groter bij patiënten die eerder hypertensie hadden ontwikkeld tijdens een zwangerschap of bij patiënten met een familiegeschiedenis van hypertensie. Hoewel de bloeddrukstijging meestal mild is, kan kwaadaardige hypertensie optreden.25 Het belangrijkste punt van zorg bij een door orale anticonceptiva veroorzaakte bloeddrukstijging is de ontwikkeling van persisterende hypertensie en daaropvolgende vroegtijdige hart- en vaatziekten, vooral bij vrouwen die roken. Stoppen met de therapie leidt meestal binnen twee tot twaalf maanden tot een terugkeer naar de uitgangswaarde van de bloeddruk, maar proteïnurie kan persisteren.25,26
De mechanismen die verantwoordelijk zijn voor het hypertensieve effect van orale anticonceptiva worden slecht begrepen. Het renine-angiotensinesysteem kan erbij betrokken zijn, omdat oestrogeen de leverproductie van het reninesubstraat angiotensinogeen stimuleert.27 Zowel oestrogeen als progesteron lijken op een dosisafhankelijke manier bij te dragen. De vaak genoemde 5% incidentie van hypertensie in verband met oestrogeen is afgeleid van onderzoeken naar hooggedoseerde therapie waarbij de oestrogeendosis ten minste 50 mcg was en de progestinedosis 1 tot 4 mg.24 De huidige preparaten bevatten echter slechts 20% van de hoeveelheid oestrogeen en progestageen die in eerdere preparaten werd gebruikt. Een rapport van de Nurses’ Health Study evalueerde prospectief bijna 70.000 vrouwelijke verpleegsters in de leeftijd van 25 tot 42 jaar.28 Na correctie voor leeftijd, gewicht, roken, familiegeschiedenis en andere risicofactoren was het relatieve risico op hypertensie bij de verpleegsters in vergelijking met vrouwen die nooit orale anticonceptiemiddelen gebruikten 1,8 voor huidige gebruiksters en 1,2 voor eerdere gebruiksters. In totaal konden slechts 41,5 gevallen van hypertensie per 10.000 persoonsjaren worden toegeschreven aan het gebruik van orale anticonceptiemiddelen, en dit aantal nam snel af met het staken van de therapie. In een meta-analyse van 14 studies, gepubliceerd tussen 1980 en 2003, was het relatieve risico van een beroerte of hartaanval twee keer zo hoog bij huidige gebruikers van orale anticonceptiva (<50 mcg ethinyl oestradiol per dag).29
Postmenopauzale oestrogeenvervangingstherapie (ERT), of hormoonvervangingstherapie (HRT) in combinatie met progestine, bestaat uit veel lagere oestrogeendoses dan die in orale anticonceptiemiddelen. ERT en HRT lijken een neutraal effect op de bloeddruk te hebben, zoals wordt geïllustreerd door de volgende waarnemingen uit twee grote gerandomiseerde onderzoeken. Het Women’s Health Initiative (WHI) is het grootste (N = 16.000) gerandomiseerde, placebogecontroleerde onderzoek dat het effect van oestrogeen-progestageenvervanging op de resultaten bij postmenopauzale vrouwen heeft geëvalueerd.30 Na 5,2 jaar veroorzaakte HRT slechts een kleine stijging (1,5 mmHg) van de systolische bloeddruk in vergelijking met placebo. Vergelijkbare bevindingen werden waargenomen in het PEPI-onderzoek waarin ERT, met of zonder progestativa, na drie jaar geen effect had op de bloeddruk.31
Extra studies waarbij minder vrouwen betrokken waren, hebben een verlaging van de ambulante bloeddruk en een grotere daling van de nachtelijke druk bij ERT-gebruiksters gevonden.32,33 Het is mogelijk dat HRT de stijging van de systolische druk over een langere behandelingsperiode vertraagt.34 Vanwege de significante toename van het risico op coronaire hartziekten, beroertes en veneuze trombo-embolieën, zoals aangetoond in de WHI, wordt HRT niet langer aanbevolen voor cardiovasculaire bescherming.35
Voedingssupplementen
Ginseng wordt algemeen beschouwd als veilig en wordt in verband gebracht met weinig ernstige bijwerkingen. Omdat het een licht stimulerend effect kan hebben, is voorzichtigheid geboden bij gebruik in combinatie met andere stimulerende middelen bij patiënten met hart- en vaatziekten. Er is een soort ginseng-misbruiksyndroom beschreven, dat wordt gekenmerkt door diarree, hypertensie, nervositeit, dermatologische erupties en slapeloosheid.36 Dit syndroom kan optreden na eenmalige hoge doses of na langdurig gebruik. Andere supplementen die de bloeddruk kunnen verhogen zijn onder meer natuurlijke zoethout en yohimbine.37 In het algemeen moeten alle patiënten met hypertensie het gebruik van voedingssupplementen vooraf met hun apotheker of arts bespreken. De effecten van de meeste supplementen op de bloeddruk zijn onvoldoende gekarakteriseerd.
Serotonine-Noradrenaline Heropnameremmers
Venlafaxine: Venlafaxine is een serotonine-noradrenaline heropnameremmer (SNRI) die wordt gebruikt bij de behandeling van depressie en angststoornissen. Het waarschijnlijke mechanisme van venlafaxine-geïnduceerde hypertensie is de toename van noradrenerge neurotransmissie.38 De venlafaxine-formule met verlengde afgifte verhoogt de bloeddruk bij ongeveer 3% van de patiënten wanneer normale doses (75-150 mg) worden gebruikt.38 De meerderheid van deze bloeddrukverhogingen werd echter als gering beschouwd. Doseringen >=300 mg venlafaxine met verlengde afgifte vertoonden klinisch significante verhogingen bij 13% van de patiënten, waarbij de meerderheid van de bloeddrukverhogingen tussen 10 en 15 mmHg lag.39 Het is echter belangrijk op te merken dat doseringen van 300 mg of meer niet gebruikelijk zijn, en dat het risico van venlafaxine-geïnduceerde hypertensie gewoonlijk niet het staken van dit geneesmiddel rechtvaardigt.40
Sibutramine: De klinische betekenis van door sibutramine veroorzaakte hypertensie is niet goed gedefinieerd. Sibutramine is een SNRI en is chemisch vergelijkbaar met amfetamine. Het waarschijnlijke mechanisme van bloeddrukverhoging door sibutramine bij zowel normotensieve als hypertensieve patiënten is de verhoogde hoeveelheid noradrenaline in het lichaam.41 Een klinisch onderzoek naar de bijwerkingen van sibutramine toonde een gemiddelde verhoging van de systolische en diastolische bloeddruk van 2 mmHg aan bij voorheen normotensieve patiënten die dagelijks 10 tot 15 mg sibutramine kregen. Interessant genoeg werd een verhoging van 7 mmHg aangetoond bij patiënten met hypertensie die een vergelijkbare dosis kregen.42 Andere onderzoeken hebben soortgelijke bevindingen aangetoond.43,44 Bij patiënten met bestaande hypertensie die sibutramine kregen, waren de bloeddrukverhogingen aanzienlijk hoger dan bij patiënten die een normale bloeddruk hadden voordat zij met de medicatie begonnen. Behandeling met sibutramine moet waarschijnlijk worden beperkt tot patiënten die geen hart- en vaatziekten hebben, waaronder hypertensie, functionele afwijkingen en coronaire hartziekte.
Immunosuppressiva
Cyclosporine: Het ongunstige effect van cyclosporine op de bloeddruk is bekend.45 Het exacte mechanisme van cyclosporine-geïnduceerde hypertensie is onzeker, maar er zijn verschillende hypothesen voorgesteld, waaronder verhoogde prostaglandinesynthese en verminderde water-, natrium- en kaliumexcretie.46,47 Tot 50% van de niertransplantatiepatiënten die met cyclosporine werden behandeld, meldden verhoogde bloeddruk, en in de meeste van deze gevallen was behandeling voor hypertensie nodig.48 Vanwege de nadelige effecten van cyclosporineontwenning bij transplantatiepatiënten en bij patiënten met auto-immuunziekten, wordt cyclosporine zelden gestaakt vanwege verhoogde hypertensie. Behandeling van cyclosporine-geïnduceerde hypertensie kan farmacologisch zijn, eventueel bestaande uit calciumkanaalblokkers, diuretica, bètablokkers of ACE-remmers, of niet-farmacologisch, bestaande uit een verminderde natriuminname.45 In 1999 werd een consensusverklaring uitgebracht, waarin staat dat als de systolische bloeddruk twee keer achter elkaar boven de 140 mmHg of de diastolische druk boven de 90 mmHg stijgt, de cyclosporinedosis met 25% moet worden verlaagd.48 Gedurende de eerste drie maanden van de cyclosporinetherapie moet de bloeddruk elke twee weken worden gecontroleerd om te controleren of er veranderingen zijn.
Tacrolimus: Bij patiënten met ernstige, therapieresistente cyclosporine-geïnduceerde hypertensie, kan overschakeling op tacrolimus een optie zijn. Van tacrolimus is aangetoond dat het, net als cyclosporine, een aanzienlijk effect heeft op de bloeddruk. De incidentie van door tacrolimus veroorzaakte hypertensie (35%) is echter lager dan die van cyclosporine (50%).49 Er wordt aangenomen dat het mechanisme van door tacrolimus veroorzaakte hypertensie vergelijkbaar is met dat van cyclosporine, zoals eerder besproken.50 Er kunnen farmacologische of niet-farmacologische aanpassingen nodig zijn, vergelijkbaar met die welke zijn vermeld voor door cyclosporine veroorzaakte hypertensie, om de bloeddrukstijgingen te behandelen die gepaard gaan met tacrolimustherapie.51 Zorgvuldige controle van de bloeddruk is geboden tijdens de behandeling met tacrolimus of cyclosporine.
Samenvattend
Pharmaceuten dienen zich bewust te zijn van de belangrijkste klassen geneesmiddelen die de bloeddruk kunnen verhogen en/of effectieve bloeddrukcontrole kunnen verstoren. Voorbeelden hiervan zijn sympathomimetica, NSAID’s, oestrogenen, corticosteroïden, cyclosporine, en sommige natuurlijke producten (bijv. ginseng). Apothekers moeten screenen op bloeddrukverhogende medicatie en feedback geven aan patiënten en zorgverleners om deze potentiële oorzaak van secundaire hypertensie te verminderen. In het algemeen moeten alle patiënten met hypertensie nauwlettender in de gaten worden gehouden wanneer extra medicijnen worden voorgeschreven, vooral wanneer er medicijnen aan worden toegevoegd waarvan bekend is dat ze de bloeddruk verhogen.
1. Cantu C, Arauz A, Murillo-Bonilla LM, et al. Stroke associated with sympathomimetics contained in over-the-counter cough and cold drugs. Stroke. 2003;34:1667-1672.
2. Kernan W, Viscoli C, Brass L, et al. Phenylpropanolamine and the risk of hemorrhagic stroke. N Engl J Med. 2000;343:1826-1832.
3. Fleming GA. De FDA, regelgeving en het risico van beroerten. N Engl J Med. 2000;343:1886-1887.
4. Mersfelder TL. Fenylpropanolamine en beroerte: de studie, de uitspraak van de FDA, de implicaties. Cleveland Clin J Med. 2001;68:213-219.
5. Salerno SM, Jackson JL, Berbano EP. Effect van oraal pseudo-efedrine op bloeddruk en hartslag: een meta-analyse. Arch Intern Med. 2005;165:1686-1694.
6. Coates ML, Rembold CM, Farr BM. Does pseudoephedrine increase blood pressure in patients with controlled hypertension? J Fam Pract. 1995;40:22-26.
7. Bradley JG. Medicijnen zonder recept en hypertensie. Welke beïnvloeden de bloeddruk? Postgrad Med.1991;89:195-197,201-202.
8. 2006 safety alerts for drugs, biologics, medical devices, and dietary supplements. Dexedrine (dextroamfetaminesulfaat). FDA. 21 augustus 2006. www.fda.gov/medwatch/safety/2006/safety06.htm#Dexedrine. Geraadpleegd op 13 mei 2008.
9. Samuels JA, Franco K, Wan F, Sorof JM. Effect of stimulants on 24-h ambulatory blood pressure in children with ADHD: a double-blind, randomized, cross-over trial. Pediatr Nephrol. 2006;21:92-95.
10. Howard PA, Delafontaine P. Nonsteroidal anti-inflammatory drugs and cardiovascular risk. J Am Coll Cardiol. 2004;43:519-525.
11. Armstrong EP, Malone DC. The impact of nonsteroidal anti-inflammatory drugs on blood pressure, with an emphasis on newer agents. Clin Ther. 2003;25:1-18.
12. Schnitzer TJ. Cyclooxygenase-2-specifieke remmers: zijn ze veilig? Am J Med. 2001;110:46S-49S.
13. DeMaria AN, Weir MR. Coxibs–beyond the GI tract: renal and cardiovascular issues. J Pain Symptom Manage. 2003;25(suppl 2):S41-S49.
14. Stollberger C, Finsterer J. Bijwerkingen van conventionele niet-steroïde anti-inflammatoire geneesmiddelen en celecoxib: meer overeenkomsten dan verschillen. South Med J. 2004;97:209.
15. Fitzgerald GA. Coxibs en hart- en vaatziekten. N Eng J Med. 2004;351:1709-1711.
16. Aw TJ, Haas SJ, Liew D, Krum H. Meta-analyse van COX-2 remmers en hun effecten op de bloeddruk. Arch Intern Med. 2005;165:490-496.
17. Merck kondigt vrijwillige wereldwijde terugtrekking van VIOXX aan. 30 september 2004. www.merck.com/newsroom/vioxx/pdf/vioxx_press_release_final.pdf. Accessed May 13, 2008.
18. de Leeuw PW. Door geneesmiddelen veroorzaakte hypertensie. Herkenning en behandeling bij oudere patiënten. Drugs Aging. 1997;11:178-185.
19. Clyburn EB, DiPette DJ. Hypertension induced by drugs and other substances. Semin Nephrol. 1995;15:72-86.
20. Hari P, Bagga A, Mantan M. Short term efficacy of intravenous dexamethasone and methylprednisolone therapy in steroid resistant nephrotic syndrome. Indian Pediatr. 2004;41:993-1000.
21. Ferrari P. Cortisol and the renal handling of electrolytes: role in glucocorticoid-induced hypertension and bone disease. Best Pract Res Clin Endocrinol Metab. 2003;17:575-589.
22. Hussain RM, McIntosh SJ, Lawson J, et al. Fludrocortisone in the treatment of hypotensive disorders in the elderly. Heart. 1996;76:507-509.
23. Noordzij M, Uiterwaal CS, Arends LR, et al. Blood pressure response to chronic intake of coffee and caffeine: a meta-analysis of randomized controlled trials. J Hypertens. 2005;23:921-928.
24. Woods JW. Orale anticonceptiva en hypertensie. Hypertension. 1988;11:II11-II15.
25. Lim KG, Isles CG, Hodsman GP. Malignant hypertension in women of childbearing age and its relation to the contraceptive pill. Br Med J (Clin Res Ed). 1987;294:1057-1059.
26. Ribstein J, Halimi JM, du Cailar G, Mimran A. Renal characteristics and effect of angiotensin suppression in oral contraceptive users. Hypertension. 1999;33:90-95.
27. Goldhaber SZ, Hennekens CH, Spark RF, et al. Plasma renine substraat, renine activiteit, en aldosteron niveaus in een steekproef van orale anticonceptie gebruiksters uit een community survey. Am Heart J. 1984;107:119-122.
28. Chasan-Taber L, Willett WC, Manson JE, et al. Prospective study of oral contraceptives and hypertension among women in the United States. Circulation. 1996;94:483-489.
29. Baillargeon JP, McClish DK, Essah PA, Nestler JE. Association between the current use of low-dose oral contraceptives and cardiovascular arterial disease: a meta-analysis. J Clin Endocrinol Metab. 2005;90:3863-3870.
30. Rossouw JE, Anderson GL, Prentice RL, et al. Risks and benefits of oestrogeen plus progestin in healthy postmenopausal women: principal results from the Women’s Health Initiative randomized controlled trial. JAMA. 2002;288:321-333.
31. Effecten van oestrogeen of oestrogeen/progestine schema’s op risicofactoren voor hartziekten bij postmenopauzale vrouwen. De Postmenopauzale Oestrogeen/Progestine Interventies (PEPI) Trial. JAMA. 1995;273:199-208.
32. Butkevich A, Abraham C, Phillips RA. Hormoonvervangende therapie en 24-uurs bloeddrukprofiel bij postmenopauzale vrouwen. Am J Hypertens. 2000;13:1039-1041.
33. Cagnacci A, Rovati L, Zanni A, et al. Fysiologische doses oestradiol verlagen de nachtelijke bloeddruk bij normotensieve postmenopauzale vrouwen. Am J Physiol.1999;276:H1355-H1360.
34. Scuteri A, Bos AJ, Brant LJ, et al. Hormoonvervangende therapie en longitudinale veranderingen in bloeddruk bij postmenopauzale vrouwen. Ann Intern Med. 2001;135:229-238.
35. Bath PM, Gray LJ. Association between hormone replacement therapy and subsequent stroke: a meta-analysis. BMJ. 2005;330:342.
36. Chen KJ. De werking en het misbruiksyndroom van ginseng. J Trad Chin Med. 1981;1:69-72.
37. Pittler MH, Schmidt K, Ernst E. Adverse events of herbal food supplements for body weight reduction: systematic review. Obes Rev. 2005;6:93-111.
38. Thase ME. Effects of venlafaxine on blood pressure: a meta-analysis of original data from 3744 depressed patients. J Clin Psychiatry. 1998;59:502-508.
39. Effexor XR (venlafaxine HCl) bijsluiter. Philadelphia, PA: Wyeth Pharmaceuticals; februari 2008.
40. Venlafaxine: een nieuwe dimensie in antidepressieve farmacotherapie. J Clin Psychiatr. 1993;54:119-126.
41. Lean ME. Sibutramine: een overzicht van de klinische werkzaamheid. Int J Obes Relat Metab Disord. 1997;21(suppl 1):S30-S36.
42. Weintraub M, Rubio A, Golik A, et al. Sibutramine in weight control: a dose-ranging, efficacy study. Clin Pharmacol Ther. 1991;50:330-337.
43. King DJ, Devaney N. Clinical pharmacology of sibutramine hydrochloride, a new antidepressant, in healthy volunteers. Br J Clin Pharmacol. 1988;26:607-611.
44. Perrio MJ, Wilton LV, Shakir SA. The safety profiles of orlistat and sibutramine: results of prescription-event monitoring studies in England. Obesitas. 2007;15:2712-2722.
45. Vercauteren SB, Bosmans JL, Elseviers MM, et al. A meta-analysis and morphological review of cyclosporine-induced nephrotoxicity in auto-immune diseases. Kidney Int. 1998;54:536-545.
46. Kutkuhn B, Hollenbeck M, Heering P, et al. Ontwikkeling van insulineresistentie en verhoogde bloeddruk tijdens therapie met cyclosporine A. Blood Press. 1997;6:13-17.
47. Charnick SB, Nedelman JR, Chang CT, et al. Beschrijving van bloeddrukveranderingen bij patiënten die beginnen met cyclosporine A therapie. Ther Drug Monit. 1997;19:17-24.
48. Cush JJ, Tugwell P, Weinblatt M, Yocum D. US consensus guidelines for use of cyclosporin A in rheumatoid arthritis. J Rheumatol. 1999;26:1176-1186.
49. Pham S, Kormos R, Hattler B, et al. Een prospectieve trial van tacrolimus bij klinische harttransplantatie: tussentijdse resultaten. J Thorac Cardiovasc Surg. 1996;111:764-772.
50. Fung JJ, Todo S, Jain A, et al. Conversie van cyclosporine naar FK 506 bij ontvangers van een leverallograft met cyclosporine-gerelateerde complicaties. Transplant Proc. 1990;22:6-12.
51. Jain A, Reyes J, Kashyap R, et al. Levertransplantatie onder tacrolimus bij zuigelingen, kinderen, volwassenen en senioren: langetermijnresultaten, overleving, en bijwerkingen bij 1000 opeenvolgende patiënten. Transplant Proc.1998;30:1403-1404.
Neem voor commentaar op dit artikel contact op met [email protected].