Ectasia dell’arteria coronaria: un dilemma del cardiologo interventista
L’ectasia dell’arteria coronaria è definita come una dilatazione localizzata o diffusa del lume dell’arteria coronaria. L’ectasia dell’arteria coronaria è ben riconosciuta, ma è un reperto raro che si incontra durante l’angiografia coronarica diagnostica. L’ectasia dell’arteria coronaria rappresenta una forma di malattia aterosclerotica dell’arteria coronaria, vista in 1.4-4.9% dei pazienti sottoposti ad angiografia coronarica. Può essere un reperto isolato o in combinazione con lesioni stenotiche.
La classificazione dell’ectasia coronarica è divisa in quattro gruppi: Tipo 1: ectasia diffusa di due o tre vasi, Tipo 2: ectasia diffusa in un vaso e malattia localizzata in un altro vaso, Tipo 3: ectasia diffusa in un solo vaso, e Tipo 4: coinvolgimento localizzato o segmentale.
Questo caso illumina il difficile processo decisionale riguardante lo stenting delle arterie coronarie con ectasia e aterosclerosi. La sfida aggiuntiva è se il beneficio dell’anticoagulazione con warfarin supera il rischio di sanguinamento. L’approccio al trattamento è spesso ambiguo, e può essere una questione clinica fastidiosa, come identificato nella nostra presentazione del caso.
Parole chiave
Ectasia dell’arteria coronaria, aneurisma coronarico, trombo, stenting, anticoagulazione
Introduzione
L’ectasia dell’arteria coronaria (CAE) è definita come una dilatazione localizzata o diffusa del lume dell’arteria coronaria che supera di 1,5 volte il diametro maggiore di un vaso coronarico normale adiacente. Il CAE è ben riconosciuto, ma è un risultato non comune incontrato durante l’angiografia coronarica diagnostica. La classificazione di CAE è divisa in quattro gruppi: Tipo 1: ectasia diffusa di due o tre vasi, Tipo 2: ectasia diffusa in un vaso e malattia localizzata in un altro vaso, Tipo 3: ectasia diffusa in un solo vaso, e Tipo 4: coinvolgimento localizzato o segmentale.
Il termine ‘ectasia’ si riferisce alla dilatazione diffusa di un’arteria coronaria, mentre la dilatazione coronarica focale è chiamata ‘un aneurisma coronarico’ . L’esatta fisiopatologia della CAE è sconosciuta. La CAE è una variante anatomica e un’espressione fenotipica della malattia coronarica che può presentarsi con ischemia miocardica o sindrome coronarica. L’incidenza varia tra 1,2-4,9%. Il registro CASS ha trovato CAE nel 4,9% degli angiogrammi coronarici. Il nostro gruppo classifica il CAE come piccolo (dimensione del vaso 8 m). Il CAE è definito come una dilatazione del lume dell’arteria coronaria con un diametro di 1,5 volte l’arteria coronaria normale adiacente sulla base del registro CASS.
Eziologia
L’eziologia del CAE può essere enigmatica. L’aterosclerosi è considerata la principale causa eziologica responsabile di oltre il 50% dei casi negli adulti, mentre la malattia di Kawasaki è la causa più comune nei bambini e nei giovani adulti. L’istologia dell’aterosclerosi e dell’ectasia sono comparabili. Il meccanismo di dilatazione luminale in alcuni vasi aterosclerotici è ambiguo; l’aterosclerosi causa tipicamente un restringimento del lume del vaso. La dilatazione luminale dovuta al rimodellamento arterioso di alcune placche si traduce in un’espansione della media e della membrana elastica esterna. Questa metodologia proposta di rimodellamento arterioso può essere operativa nel caso della CAE.
L’ecografia intravascolare rivela che il rimodellamento arterioso può essere bidirezionale a seconda dell’espansione o della contrazione della membrana elastica esterna. Si ritiene che la CAE sia un esagerato rimodellamento espansivo della membrana elastica esterna con conseguente espansione luminale. La degradazione enzimatica della matrice extracellulare da parte delle metalloproteinasi di matrice e di altri enzimi litici e l’assottigliamento della tunica media associata a una grave infiammazione cronica è considerata la patogenesi principale del rimodellamento espansivo. La CAE è anche legata all’HCM apicale con alta tensione di parete. La formazione di aneurismi può essere vista dopo interventi coronarici percutanei tra cui l’angioplastica con palloncino, il posizionamento di stent e l’aterectomia. Si ritiene che il meccanismo sia la lesione della media del vaso sanguigno.
Diagnosi
L’angiografia coronarica è il gold standard nella diagnosi della CAE. L’ecografia intravascolare (IVUS) è fondamentale per la valutazione delle caratteristiche luminali e delle patologie. Le distorsioni del flusso coronarico e il washout sono comuni nella CAE e sono correlati alla gravità dell’ectasia. Segni di flusso stagnante includono: Riempimento ritardato di contrasto anterogrado, reflusso segmentale e stasi nel segmento coronarico ectatico.
Significato clinico
I sintomi possono essere associati a malattia coronarica concomitante, malattia di Kawasaki o malattia del tessuto connettivo. La maggior parte dei pazienti sono asintomatici. I pazienti con CAE possono presentare angina, test da sforzo positivi e sindrome coronarica acuta. La diminuzione del flusso coronarico, o il ristagno del flusso sanguigno, può causare angina indotta dall’esercizio senza una malattia coronarica stenotica coesistente. La formazione di un trombo intracoronarico e la dissipazione degli emboli distalmente possono essere l’innesco della sindrome coronarica acuta, che è accelerata dal flusso stagnante nel segmento coronarico ectatico. La CAE è predisposta al vasospasmo, che può provocare angina o sindrome coronarica acuta. Nelle persone con meno di 50 anni la CAE dovrebbe suscitare una preoccupazione per i disturbi del tessuto connettivo e le vasculiti.
Prognosi
La prognosi della CAE è direttamente correlata alla gravità della malattia coronarica concomitante. La CAE con la malattia coronarica sottostante è una combinazione dannosa con un potenziale aumentato di eventi cardiaci avversi. La CAE isolata comporta ancora il rischio di ischemia e infarto miocardico. La CAE di tipo 1 e di tipo 2 comporta un rischio maggiore rispetto alla CAE di tipo 3 e di tipo 4. Non ci sono dati riportati che mostrano una relazione tra il diametro di un’arteria e il risultato.
Trattamento
La gestione della CAE è irta di incertezze perché la rarità della CAE impedisce grandi studi randomizzati che confrontano diversi approcci di trattamento. Quando la CAD coesiste, un’intensa modifica dei fattori di rischio primari e secondari è obbligatoria.
La gestione della CAE isolata in caso di angina o ischemia miocardica comprende ASA, statina e farmaci anti-ischemici. Le sindromi coronariche acute associate a CAE possono richiedere la trombolisi, la somministrazione di eparina e gli inibitori del recettore della glicoproteina 2b/3a. L’aspirazione del trombo può essere necessaria durante la PCI primaria. Gli interventi percutanei e chirurgici sono spesso necessari nei pazienti con CAE e lesioni stenotiche in cui l’angina persiste nonostante la terapia medica massima. Il dimensionamento ottimale dello stent, l’errato posizionamento e l’embolizzazione degli stent, la trombosi precoce dello stent e la restenosi tormentano le procedure di stenting.
L’anticoagulazione a lungo termine è un argomento dibattuto, senza studi randomizzati che conferiscano un beneficio. Il beneficio antipiastrinico deve essere soppesato rispetto al rischio di emorragia.
Caso
Un uomo afroamericano di 51 anni si è presentato al pronto soccorso con dolore al petto. È stato trovato con una troponina elevata. Il livello di troponina nel sangue era 0,45 (
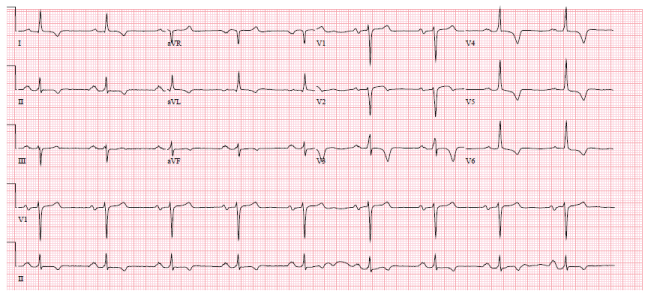 Figura 1: Ritmo sinusale, asse sinistro, e onde t invertite 1, 2 aVL, V 3-6. Vedi Figura 1
Figura 1: Ritmo sinusale, asse sinistro, e onde t invertite 1, 2 aVL, V 3-6. Vedi Figura 1
Quattro anni prima il paziente aveva sperimentato un’occlusione acuta della sua coronaria discendente anteriore sinistra prossimale (LAD). Egli è stato sottoposto a trombectomia e stenting LAD prossimale (Figura 2a e Figura 2b).
 Figura 2: a) vista angiogramma coronarico LAO rivelando occlusa LAD prossimale (2014); b) angiogramma coronarico RAO post trombectomia e posizionamento di uno stent 4.0*22 resolute (2014). Vedi Figura 2
Figura 2: a) vista angiogramma coronarico LAO rivelando occlusa LAD prossimale (2014); b) angiogramma coronarico RAO post trombectomia e posizionamento di uno stent 4.0*22 resolute (2014). Vedi Figura 2
Durante l’angiografia è stata identificata la CAE di tipo 1. L’arteria coronaria destra (RCA), arteria coronaria circonflessa (Cf) e LAD erano tutti grandi vasi luminali coerenti con ectasia coronarica. (Figura 3 e Figura 4) Il paziente ha avuto un episodio sintomatico di tachicardia ventricolare che era emodinamicamente compromettente ed è stato gestito con cardioversione. Il paziente si è ripreso ed è stato trattato con ASA e ticagrelor per 18 mesi e poi è passato al solo ASA. È rimasto attivo e libero da sintomi cardiovascolari.
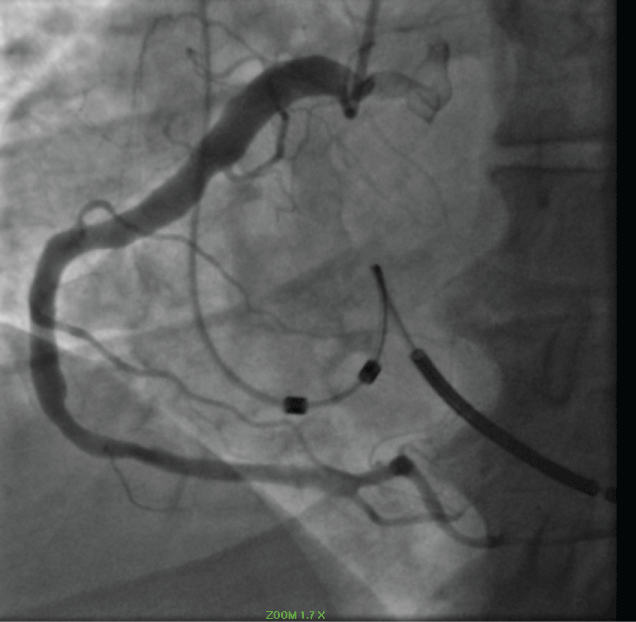 Figura 3: Coronaria destra ectatica. Vedi Figura 3
Figura 3: Coronaria destra ectatica. Vedi Figura 3
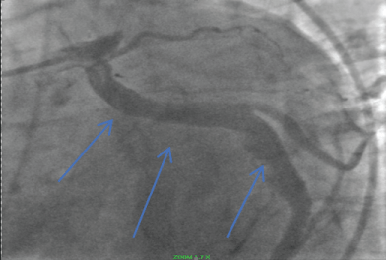 Figura 4: Arteria coronaria circonflessa ectatica (frecce blu). Vedi Figura 4
Figura 4: Arteria coronaria circonflessa ectatica (frecce blu). Vedi Figura 4 Anamnesi medica passata: Il paziente ha una storia di cardiomiopatia ipertrofica (HCM) gene-negativa. Nel 1983 all’età di 16 anni ha avuto un episodio sincopale mentre giocava a basket ed è stato identificato come affetto da CMI mediante ecocardiografia (Figura 5, Figura 6, Figura 7 e Figura 8). Nel 2002 il paziente ha avuto un altro episodio sincopale ed è stato trovato con una tachicardia ventricolare non sostenuta sul monitoraggio Holter. Gli fu impiantato un ICD. Aveva ipertensione, malattia coronarica, HCM, iperlipidemia, sincope, NSVT e VT post infarto miocardico che è stato gestito con terapia d’urto.
 Figura 5: L’asse lungo parasternale del LV che rivela un setto di 17 mm in un paziente con HCM. Visualizza Figura 5
Figura 5: L’asse lungo parasternale del LV che rivela un setto di 17 mm in un paziente con HCM. Visualizza Figura 5
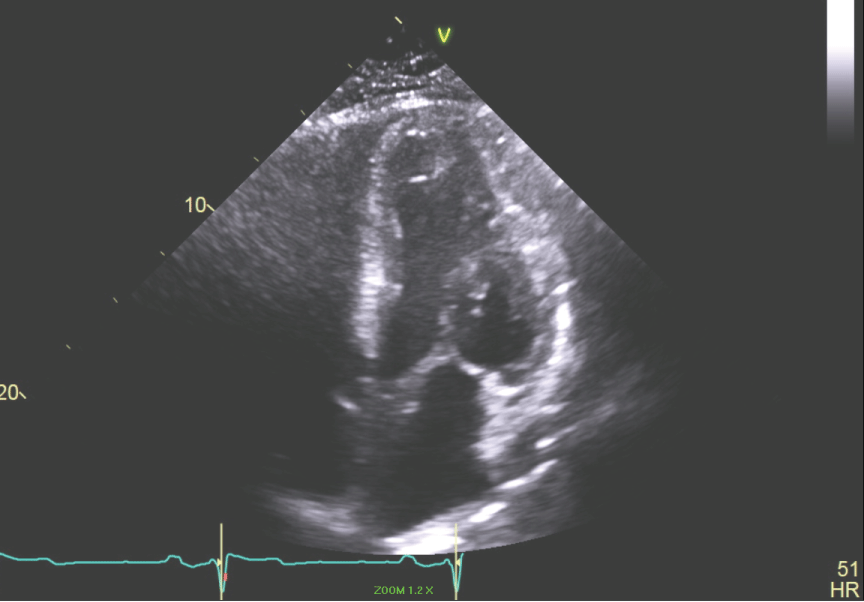 Figura 6: Vista apicale 4 camere del LV che mostra piccola cavità LV. Visualizza Figura 6
Figura 6: Vista apicale 4 camere del LV che mostra piccola cavità LV. Visualizza Figura 6 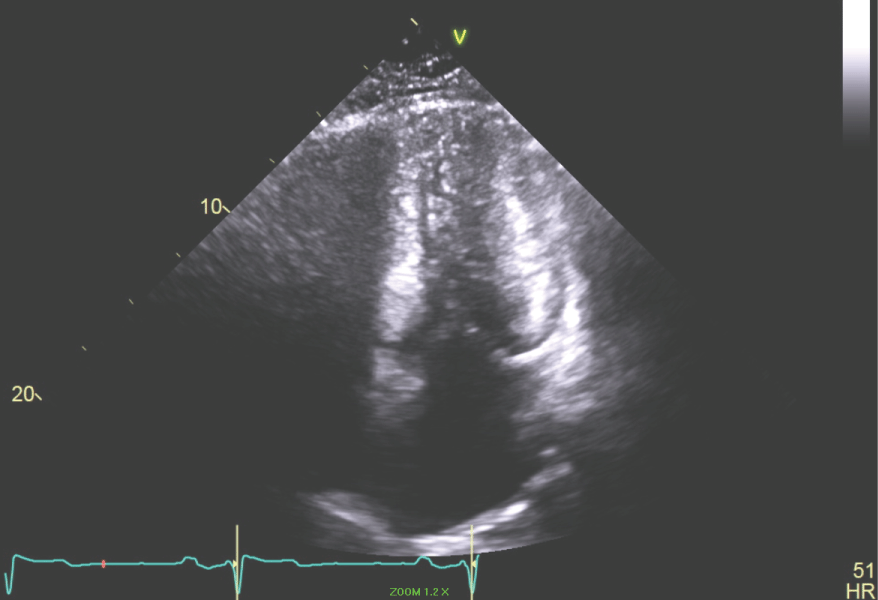 Figura 7: Vista apicale 4 camere del LV che mostra la dimensione sistolica fine con LV cavità obliterazione. Visualizza Figura 7
Figura 7: Vista apicale 4 camere del LV che mostra la dimensione sistolica fine con LV cavità obliterazione. Visualizza Figura 7
 Figura 8: ceppo sistolico di picco del LV rivelando diminuisce anteriore, medio, e inferiore ceppo settale. Vedi Figura 8
Figura 8: ceppo sistolico di picco del LV rivelando diminuisce anteriore, medio, e inferiore ceppo settale. Vedi Figura 8
Anamnesi familiare: Era positivo per CAD precoce con suo padre che è morto di infarto miocardico all’età di 56 anni e sua madre che ha subito un bypass coronarico all’età di 56 anni.
Esame fisico: Rivela un maschio nero ben sviluppato con una pressione sanguigna di 130/70 mmHg e un polso di 48 bpm. JVP: normale, risalita carotidea: S1, S2, S4 e mormorio di eiezione sistolica 1/6 normali e pulsazioni palpabili alle estremità superiori e inferiori.
La presentazione del 2018 era coerente con un NSTEMI. L’angiografia coronarica ha rivelato una RCA brevettata (Figura 9).
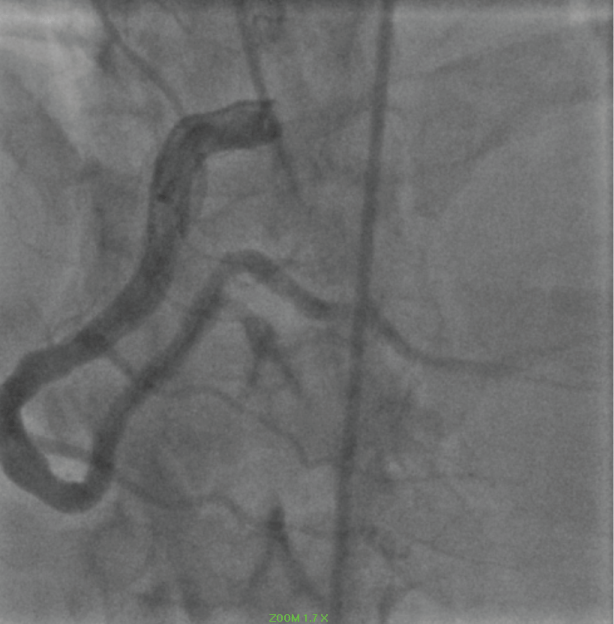 Figura 9: RCA ectatica. View Figure 9
Figura 9: RCA ectatica. View Figure 9
Trombo è stato identificato in un’arteria coronaria circonflessa ectatica (Figura 10).
 Figura 10: Trombo circonflesso: contorno rosso 2018. Visualizza Figura 10
Figura 10: Trombo circonflesso: contorno rosso 2018. Visualizza Figura 10
Trombo è stato identificato nella LAD (Figura 11).
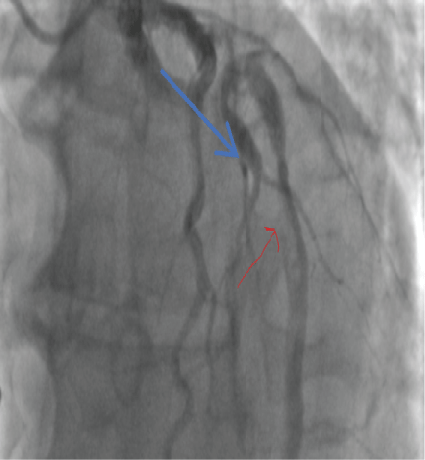 Figura 11: coagulo LAD (freccia blu) 2018. Visualizza Figura 11
Figura 11: coagulo LAD (freccia blu) 2018. Visualizza Figura 11
Il paziente è stato trattato per 72 ore con aspirina e ticagrelor. La speranza era di sciogliere il trombo e determinare il grado di aterosclerosi sottostante.
L’angiografia di follow-up ha rivelato che il carico del trombo nella circonflessa e nella LAD era invariato. Il paziente non aveva altri sintomi clinici. L’aspirina è stata continuata e l’eparina è stata iniziata. Inoltre, il paziente è stato avviato alla terapia con warfarin dopo aver discusso i rischi e i benefici. Una volta che l’INR era 2,5, il paziente è stato dimesso per il follow-up.
Discussione
Le opzioni di trattamento per la CAE includono la modifica dei fattori di rischio, la terapia anti-ischemica, l’ASA e la terapia antitrombotica. Molti autori raccomandano l’anticoagulazione cronica, ma nessuno studio randomizzato dimostra il suo beneficio nella CAE. Il beneficio previsto deve essere controbilanciato dal rischio di emorragia.
In questo caso, la formazione ricorrente di trombi nelle arterie coronarie ectatiche di tipo 1 ha posto il paziente ad alto rischio di ischemia ricorrente e infarto miocardico. Il profilo ad alto rischio di questo paziente ha reso accettabile il riconoscimento delle complicazioni emorragiche della terapia con warfarin. Il paziente è stato dimesso con un piano per un attento monitoraggio del suo INR e dei sintomi clinici. Un test da sforzo nucleare è stato organizzato per 6 settimane.
Questo caso chiarisce il difficile processo decisionale associato allo stenting delle arterie coronarie con ectasia e aterosclerosi e l’uso di warfarin per l’anticoagulazione per prevenire la formazione di trombi coronarici. Il trattamento dell’ectasia dell’arteria coronaria con l’aterosclerosi è una domanda clinica vexing come identificato nella nostra presentazione di caso. Attualmente queste decisioni devono essere prese su base individuale.
Conflitti di interesse
Non ci sono conflitti di interesse.
Riconoscimenti
Nessun riconoscimento.
- AR Zeina, D Sharif, J Blinder, Rosenschein U, Barmeir E (2007) Valutazione non invasiva dell’arteria coronaria utilizzando la tomografia computerizzata multidetettore. Coron Artery Dis 18: 175-180.
- S Mavrogeni (2010) Coronary artery ectasia: Dalla diagnosi al trattamento. Hellenic J Cardiol 51: 158-163.
- PS Swaye, LD Fisher, P Litwin, PA Vignola, MP Judkins, et al. (1983) Aneurysmal coronary artery disease. Circulation 67: 134-138.
- Díaz-Zamudio M, Bacilio-Pérez U, Herrera-Zarza MC, Meave-González A, Alexanderson-Rosas E, et al. (2009) Coronary artery aneurysms and ectasia: Ruolo dell’angiografia CT coronarica. Radiografia 29: 1939-1954.
- AP Antoniadis, YS Chatzizsis, GD Giannoglou (2008) meccanismi patogenetici di ectasia coronarica. Int J Cardiol 130: 335-343.
- A Magginas, DV Cokkinos (2006) Ectasie coronariche: Imaging, valutazione funzionale e implicazioni cliniche. Eur Heart J 27: 1026-1031.
- Sayin T, Döven O, Berkalp B, Akyürek O, Güleç S, et al. (2001) Ischemia miocardica indotta dall’esercizio fisico in pazienti con ectasia coronarica senza malattia coronarica ostruttiva. Int J Cardiol 78: 143-149.
- Zografos TA, Korovesis S, Giazitzoglou E, Kokladi M, Venetsanakos I, et al. (2013) Caratteristiche cliniche e angiografiche dei pazienti con ectasia coronarica. Int J Cardiol 167: 1536-1541.
- S Gulec, Y Atmaca, M Kilickap, Akyürek O, Aras O, et al. (2003) Valutazione angiografica della perfusione miocardica in pazienti con ectasia coronarica isolata. Am J Cardiol 91: 996-999.
- H Turnhan, E Yetkin (2007) Qual è la strategia plausibile per la gestione dei pazienti con ectasia coronarica isolata e ischemia miocardica? Int J Cardiol 117: 285-286.
- Levine GN, Bates ER, Blankenship JC, Bailey SR, Bittl JA, et al. (2011) 2011 ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the Society for Cardiovascular Angiography and Interventions. Circolazione 124: e574-e651.