Espectroscopia de ressonância magnética nuclear

Frequência ressonanteEditar
Quando colocado num campo magnético, os núcleos activos da RMN (tais como 1H ou 13C) absorvem radiação electromagnética a uma frequência característica do isótopo. A frequência ressonante, a energia da radiação absorvida e a intensidade do sinal são proporcionais à força do campo magnético. Por exemplo, num campo magnético de 21 Tesla, os núcleos de hidrogénio (vulgarmente designados por prótons) ressoam a 900 MHz. É comum referir-se a um íman de 21 T como um íman de 900 MHz, uma vez que o hidrogénio é o núcleo mais comum detectado, no entanto, núcleos diferentes ressoarão a frequências diferentes a esta intensidade de campo, em proporção aos seus momentos magnéticos nucleares.
manipulação da amostraEditar
Um espectrómetro NMR consiste tipicamente num porta-amostra giratório dentro de um íman muito forte, um emissor de radiofrequência e um receptor com uma sonda (um conjunto de antena) que vai dentro do íman para rodear a amostra, opcionalmente bobinas gradientes para medições de difusão, e electrónica para controlar o sistema. A rotação da amostra é normalmente necessária para medir o movimento de difusão, contudo algumas experiências requerem uma amostra estacionária quando o movimento da solução é uma variável importante. Por exemplo, as medições de constantes de difusão (espectroscopia de difusão ordenada ou DOSY) são feitas usando uma amostra estacionária com spin off, e as células de fluxo podem ser usadas para análise online de fluxos de processo.
solventes deuteradosEditar
A grande maioria das moléculas numa solução são moléculas de solventes, e a maioria dos solventes regulares são hidrocarbonetos e por isso contêm protões NMR-activos. A fim de evitar detectar apenas sinais de átomos de hidrogénio solvente, são utilizados solventes deuterados onde 99+% dos prótons são substituídos por deutério (hidrogénio-2). O solvente deuterado mais utilizado é o deuteroclorofórmio (CDCl3), embora outros solventes possam ser utilizados por várias razões, tais como solubilidade de uma amostra, desejo de controlar a ligação de hidrogénio, ou pontos de fusão ou de ebulição. Os deslocamentos químicos de uma molécula mudarão ligeiramente entre solventes, e o solvente utilizado será quase sempre reportado com os deslocamentos químicos. Os espectros de RMN são frequentemente calibrados contra o pico conhecido do próton residual do solvente em vez de adicionar tetrametilsilano.
Shim and lockEdit
Para detectar os desvios de frequência muito pequenos devido à ressonância magnética nuclear, o campo magnético aplicado deve ser constante em todo o volume da amostra. Os espectrómetros NMR de alta resolução utilizam calços para ajustar a homogeneidade do campo magnético a partes por bilião (ppb), num volume de alguns centímetros cúbicos. A fim de detectar e compensar a não homogeneidade e a deriva no campo magnético, o espectrómetro mantém uma “fechadura” na frequência do deutério solvente com uma unidade de fechadura separada, que é essencialmente um transmissor adicional e um processador RF sintonizado no núcleo da fechadura (deutério), em vez dos núcleos da amostra de interesse. Nos espectrómetros modernos de RNM, a cintilação é ajustada automaticamente, embora em alguns casos o operador tenha de optimizar manualmente os parâmetros de cintilação para obter a melhor resolução possível
Aquisição de espectrosEdit
Excitação da amostra com um pulso de radiofrequência (60-1000 MHz), obtém-se uma resposta de ressonância magnética nuclear – um decaimento por indução livre (FID). É um sinal muito fraco, e requer receptores de rádio sensíveis para captar. É realizada uma transformação de Fourier para extrair o espectro de domínio de frequência do FID em bruto do domínio do tempo. Um espectro de um único FID tem uma baixa relação sinal-ruído, mas melhora prontamente com a média de aquisições repetidas. Bons espectros de 1H NMR podem ser adquiridos com 16 repetições, o que leva apenas alguns minutos. No entanto, para elementos mais pesados que o hidrogénio, o tempo de relaxamento é bastante longo, por exemplo, cerca de 8 segundos para 13C. Assim, a aquisição de espectros quantitativos de elementos pesados pode ser demorada, levando dezenas de minutos a horas.
Segundo o pulso, os núcleos estão, em média, excitados a um determinado ângulo vs. o campo magnético do espectrómetro. A extensão da excitação pode ser controlada com a largura do impulso, normalmente ca. 3-8 µs para o impulso óptimo de 90°. A largura do impulso pode ser determinada traçando a intensidade (assinada) em função da largura do impulso. Segue uma curva senoidal e, consequentemente, muda de sinal em larguras de pulso correspondentes a impulsos de 180° e 360°.
Tempos de decaimento da excitação, tipicamente medidos em segundos, dependem da eficácia do relaxamento, que é mais rápido para núcleos mais leves e em sólidos, e mais lento para núcleos mais pesados e em soluções, e podem ser muito longos em gases. Se o segundo pulso de excitação for enviado prematuramente antes do relaxamento estar completo, o vector de magnetização médio não se deteriorou até ao estado de terra, o que afecta a força do sinal de uma forma imprevisível. Na prática, as áreas de pico não são então proporcionais à estequiometria; apenas a presença, mas não a quantidade de grupos funcionais é possível de discernir. Uma experiência de recuperação da inversão pode ser feita para determinar o tempo de relaxamento e, portanto, o atraso necessário entre os impulsos. É transmitido um impulso de 180°, um atraso ajustável, e um impulso de 90°. Quando o impulso de 90° cancela exactamente o sinal, o atraso corresponde ao tempo necessário para 90° de relaxação. A recuperação da inversão vale a pena para as experiências quantitativas 13C, 2D e outras experiências demoradas.
Mudança químicaEdit
Uma carga giratória gera um campo magnético que resulta num momento magnético proporcional ao giro. Na presença de um campo magnético externo, existem dois estados de spin (para um spin 1/2 núcleo): um spin para cima e um spin para baixo, onde um se alinha com o campo magnético e o outro se opõe a ele. A diferença de energia (ΔE) entre os dois estados de spin aumenta à medida que a força do campo aumenta, mas esta diferença é normalmente muito pequena, levando à exigência de ímanes NMR fortes (1-20 T para instrumentos NMR modernos). A irradiação da amostra com energia correspondente à separação exacta do estado de centrifugação de um conjunto específico de núcleos provocará a excitação desses conjuntos de núcleos no estado de menor energia para o estado de maior energia.
Para centrifugar 1/2 núcleos, a diferença de energia entre os dois estados de centrifugação a uma dada força do campo magnético é proporcional ao seu momento magnético. No entanto, mesmo que todos os prótons tenham os mesmos momentos magnéticos, não dão sinais ressonantes com os mesmos valores de frequência. Esta diferença resulta dos diferentes ambientes electrónicos do núcleo de interesse. Ao aplicar um campo magnético externo, estes electrões movem-se em resposta ao campo e geram campos magnéticos locais que se opõem ao campo aplicado muito mais forte. Este campo local “protege” assim o protão do campo magnético aplicado, que deve por isso ser aumentado para se obter ressonância (absorção de energia rf). Tais incrementos são muito pequenos, geralmente em partes por milhão (ppm). Por exemplo, o pico do protão de um aldeído é deslocado cerca de 10 ppm em comparação com um pico de hidrocarboneto, uma vez que, como grupo de extracção de electrões, o carbonilo escapa o protão reduzindo a densidade local de electrões. A diferença entre 2,3487 T e 2,3488 T é portanto de cerca de 42 ppm. Contudo, uma escala de frequência é normalmente utilizada para designar os sinais NMR, embora o espectrómetro possa funcionar através da varredura do campo magnético, e assim os 42 ppm são 4200 Hz para uma frequência de referência de 100 MHz (rf).
No entanto, dado que a localização dos diferentes sinais NMR depende da intensidade do campo magnético externo e da frequência de referência, os sinais são geralmente relatados em relação a um sinal de referência, geralmente o de TMS (tetrametilsilano). Além disso, dado que a distribuição dos sinais de RMN depende do campo, estas frequências são divididas pela frequência do espectrómetro. Contudo, uma vez que estamos a dividir Hz por MHz, o número resultante seria demasiado pequeno, e por isso é multiplicado por um milhão. Esta operação dá, portanto, um número de localizador chamado “deslocamento químico” com unidades de partes por milhão. Em geral, os deslocamentos químicos para prótons são altamente previsíveis uma vez que os deslocamentos são principalmente determinados por efeitos de blindagem mais simples (densidade de electrões), mas os deslocamentos químicos para muitos núcleos mais pesados são mais fortemente influenciados por outros factores, incluindo estados excitados (contribuição “paramagnética” para o tensor de blindagem).

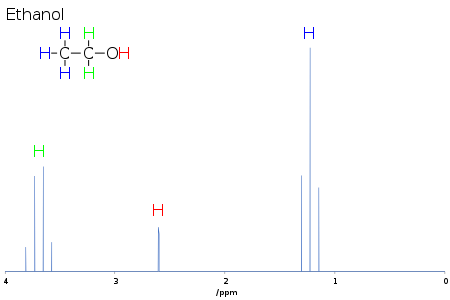
O deslocamento químico fornece informação sobre a estrutura da molécula. A conversão dos dados brutos para esta informação é chamada atribuição do espectro. Por exemplo, para o espectro 1H-NMR para etanol (CH3CH2OH), seria de esperar sinais em cada um de três turnos químicos específicos: um para o grupo CH3, um para o grupo CH2 e um para o grupo OH. Um grupo CH3 típico tem um turno de cerca de 1 ppm, um CH2 ligado a um OH tem um turno de cerca de 4 ppm e um OH tem um turno de 2-6 ppm, dependendo do solvente utilizado e da quantidade de ligação de hidrogénio. Enquanto o átomo O afasta a densidade de electrões do H ligado através da sua ligação sigma mútua, os pares solitários de electrões no O banham o H no seu efeito de protecção.
Na espectroscopia NMR paramagnética, as medições são conduzidas em amostras paramagnéticas. O paramagnetismo dá origem a deslocamentos químicos muito diversos. Na espectroscopia 1H NMR, o intervalo de deslocamento químico pode abranger até milhares de ppm.
Por causa do movimento molecular à temperatura ambiente, os três prótons de metilo saem em média durante a experiência NMR (que normalmente requer alguns ms). Estes protões degeneram e formam um pico no mesmo deslocamento químico.
A forma e a área dos picos são também indicadores da estrutura química. No exemplo acima – o espectro de prótons do etanol – o pico CH3 tem três vezes a área do pico OH. Do mesmo modo, o pico CH2 seria o dobro da área do pico OH mas apenas 2/3 da área do pico CH3.
Software permite a análise da intensidade do sinal dos picos, que em condições de relaxamento óptimo, se correlacionam com o número de protões desse tipo. A análise da intensidade do sinal é feita por integração – o processo matemático que calcula a área sob uma curva. O analista deve integrar o pico e não medir a sua altura porque os picos também têm largura – e assim o seu tamanho depende da sua área e não da sua altura. Contudo, deve ser mencionado que o número de prótons, ou qualquer outro núcleo observado, só é proporcional à intensidade, ou à integral, do sinal de RMN nas experiências de RMN unidimensionais mais simples. Em experiências mais elaboradas, por exemplo, experiências tipicamente utilizadas para obter espectros de RMN de carbono-13, a integral dos sinais depende da taxa de relaxamento do núcleo, e das suas constantes de acoplamento escalar e dipolar. Muito frequentemente estes factores são pouco conhecidos – portanto, a integral do sinal NMR é muito difícil de interpretar em experiências mais complicadas de NMR.
J-couplingEdit
| Multiplicidade | Intensity ratio |
|---|---|
| Singlet (s) | 1 |
| Doublet (d) | 1:1 |
| 1:2:1 | |
| Quartet (q) | 1:3:3:1 |
| Quintet | 1:4:6:4:1 |
| 1:5:10:10:5:1 | |
| 1:6:15:20:15:6:1 |
algumas das informações mais úteis para a determinação da estrutura num espectro NMR unidimensional vêm do acoplamento J ou do acoplamento escalar (um caso especial de acoplamento spin-spin) entre núcleos activos NMR. Este acoplamento surge da interacção de diferentes estados de spin através das ligações químicas de uma molécula e resulta na divisão dos sinais de NMR. Para um próton, o campo magnético local é ligeiramente diferente dependendo se um núcleo adjacente aponta para ou contra o campo magnético do espectrómetro, o que dá origem a dois sinais por próton em vez de um. Estes padrões de divisão podem ser complexos ou simples e, do mesmo modo, podem ser facilmente interpretáveis ou enganadores. Este acoplamento proporciona uma visão detalhada da conectividade dos átomos numa molécula.
Acoplamento a n equivalentes (spin ½) núcleos divide o sinal num n+1 multiplet com relações de intensidade seguindo o triângulo de Pascal, tal como descrito à direita. O acoplamento a giros adicionais levará a mais divisões de cada componente do multiplet, por exemplo, acoplamento a dois giros diferentes ½ núcleos com constantes de acoplamento significativamente diferentes conduzirão a um doublet de doublets (abreviatura: dd). Note-se que o acoplamento entre núcleos que são quimicamente equivalentes (ou seja, têm o mesmo deslocamento químico) não tem efeito nos espectros de RMN e os acoplamentos entre núcleos que estão distantes (geralmente mais de 3 ligações separadas para protões em moléculas flexíveis) são normalmente demasiado pequenos para causar divisões observáveis. Acoplamentos de longo alcance em mais de três ligações podem frequentemente ser observados em compostos cíclicos e aromáticos, levando a padrões de divisão mais complexos.
Por exemplo, no espectro de prótons para etanol descrito acima, o grupo CH3 é dividido em um trigémeo com uma razão de intensidade de 1:2:1 pelos dois prótons CH2 vizinhos. Da mesma forma, o CH2 é dividido num quarteto com uma razão de intensidade de 1:3:3:1 pelos três prótons CH3 vizinhos. Em princípio, os dois prótons CH2 também seriam novamente divididos num doublet para formar um doublet de quartetos pelo próton hidroxil, mas a troca intermolecular do próton hidroxil ácido resulta frequentemente numa perda de informação de acoplamento.
Acoplamento a qualquer núcleo spin-1/2 como o fósforo-31 ou o flúor-19 funciona desta forma (embora as magnitudes das constantes de acoplamento possam ser muito diferentes). Mas os padrões de divisão diferem dos descritos acima para núcleos com centrifugação superior a ½ porque o número quântico da centrifugação tem mais de dois valores possíveis. Por exemplo, o acoplamento ao deutério (um núcleo spin 1) divide o sinal num trio 1:1:1 porque o spin 1 tem três estados de spin. Da mesma forma, um núcleo spin 3/2 como o 35Cl divide um sinal num quarteto 1:1:1:1 e assim por diante.
Acoplamento combinado com o deslocamento químico (e a integração para prótons) diz-nos não só sobre o ambiente químico dos núcleos, mas também sobre o número de núcleos NMR activos vizinhos dentro da molécula. Em espectros mais complexos com picos múltiplos em turnos químicos semelhantes ou em espectros de núcleos diferentes do hidrogénio, o acoplamento é muitas vezes a única forma de distinguir diferentes núcleos.

Acoplamento de segunda ordem (ou forte)Edit
A descrição acima assume que a constante de acoplamento é pequena em comparação com a diferença nas frequências de RMN entre as rotações inequivalentes. Se a separação por turno diminui (ou a força do acoplamento aumenta), os padrões de intensidade de múltiplost são primeiro distorcidos, e depois tornam-se mais complexos e menos facilmente analisados (especialmente se estiverem envolvidas mais de duas rotações). A intensificação de alguns picos num multiplet é conseguida à custa dos restantes, que por vezes quase desaparecem no ruído de fundo, embora a área integrada sob os picos permaneça constante.Na maior parte das RMN de campo alto, contudo, as distorções são geralmente modestas e as distorções características (telhados) podem de facto ajudar a identificar os picos relacionados.
alguns destes padrões podem ser analisados com o método publicado por John Pople, embora tenha um âmbito limitado.
Os efeitos de segunda ordem diminuem à medida que a diferença de frequência entre os múltiplos aumenta, de modo que os espectros de RMN de campo alto (ou seja, de alta frequência) exibem menos distorção do que os espectros de frequência mais baixa. Os espectros iniciais a 60 MHz eram mais propensos à distorção do que os espectros de máquinas posteriores que operam tipicamente a frequências a 200 MHz ou superiores.
Outras vezes, como na figura à direita, o acoplamento J pode ser utilizado para identificar a substituição orto-meta-para de um anel. O acoplamento Ortho é o mais forte a 15 Hz, o Meta segue com uma média de 2 Hz, e finalmente o acoplamento para acoplamento é geralmente insignificante para estudos.
Iniquivalência magnéticaEdit
Mais efeitos subtis podem ocorrer se as rotações quimicamente equivalentes (ou seja, núcleos relacionados por simetria e tendo assim a mesma frequência NMR) tiverem relações de acoplamento diferentes com rotações externas. As rotações que são quimicamente equivalentes mas não são indistinguíveis (com base nas suas relações de acoplamento) são denominadas magneticamente inequivalentes. Por exemplo, os 4 H locais de 1,2-diclorobenzeno dividem-se em dois pares quimicamente equivalentes por simetria, mas um membro individual de um dos pares tem acoplamentos diferentes das rotações que compõem o outro par. A inequivalência magnética pode levar a espectros altamente complexos que só podem ser analisados por modelagem computacional. Tais efeitos são mais comuns nos espectros NMR de sistemas aromáticos e outros não flexíveis, enquanto que a média conformacional sobre as ligações C-C em moléculas flexíveis tende a equalizar os acoplamentos entre prótons em carbonos adjacentes, reduzindo os problemas com a desigualdade magnética.