Structuurisomeer
StructuurequivalentieEdit
Een molecuul (met inbegrip van polyatomische ionen) A en B hebben dezelfde structuur als elk atoom van A kan worden gepaard met een atoom van B van hetzelfde element, op een één-op-één manier, zodat er voor elke binding in A een binding in B is van hetzelfde type, tussen overeenkomstige atomen; en omgekeerd. Deze eis geldt ook voor complexe bindingen waarbij drie of meer atomen betrokken zijn, zoals de gedelokaliseerde bindingen in het benzeenmolecuul en andere aromatische verbindingen.
Afhankelijk van de context kan men eisen dat elk atoom gekoppeld is aan een atoom van dezelfde isotoop, niet alleen van hetzelfde element.
Van twee moleculen kan dan worden gezegd dat ze structurele isomeren zijn (of, als isotopen ertoe doen, structurele isotopomeren) als ze dezelfde molecuulformule hebben, maar niet dezelfde structuur.
Structurele symmetrie en equivalente atomenEdit
Structurele symmetrie van een molecuul kan wiskundig worden gedefinieerd als een permutatie van de atomen waarbij ten minste twee atomen worden uitgewisseld maar de structuur van het molecuul niet verandert. Van twee atomen kan dan worden gezegd dat ze structureel equivalent zijn als er een structurele symmetrie is die de een naar de ander overbrengt.
Zo zijn bijvoorbeeld alle vier de waterstofatomen van methaan structureel equivalent, omdat elke permutatie van die atomen alle bindingen van het molecuul in stand zal houden.
Ook alle zes waterstofatomen van ethaan (C
2H
6) zijn structureel equivalent aan elkaar, net als de twee koolwaterstoffen; omdat elke waterstof met elke andere kan worden verwisseld, hetzij door een permutatie die alleen die twee atomen verwisselt, hetzij door een permutatie die de twee koolwaterstoffen en elke waterstof in een methylgroep verwisselt met een andere waterstof op de andere methylgroep. Bij beide bewerkingen blijft de structuur van het molecuul behouden. Dat is ook het geval voor de waterstofatomen cyclopentaan, alleen, 2-butyne, hexamethyleentetramine, prismane, cubaan, dodecaëder, enz.
Aan de andere kant zijn de waterstofatomen van propaan niet allemaal structureel gelijkwaardig. De zes waterstofatomen die aan de eerste en derde koolstof vastzitten zijn gelijkwaardig, zoals in ethaan, en de twee die aan de middelste koolstof vastzitten zijn gelijkwaardig aan elkaar; maar er is geen gelijkwaardigheid tussen deze twee equivalentieklassen.
Symmetrie en positioneel isomerismeEdit
Structurele equivalenties tussen atomen van een moedermolecuul verminderen het aantal positionele isomeren dat kan worden verkregen door die atomen te vervangen voor een ander element of een andere groep. Zo betekent de structurele equivalentie tussen de zes hydrogenen van ethaan C
2H
6 dat er slechts één structurele isomeer van ethanolCH
5OH is, en niet 6. De acht hydrogenen van propaan C
3H
8 zijn verdeeld in twee structurele equivalentieklassen (de zes op de methylgroepen, en de twee op de centrale koolstof); daarom zijn er slechts twee positionele isomeren van propanol (1-propanol en 2-propanol). Evenzo zijn er slechts twee positie-isomeren van butanol, en drie van pentanol of hexanol.
Symmetriebreking door substitutiesEdit
Als een substitutie in een moedermolecuul is aangebracht, wordt de structurele symmetrie gewoonlijk gereduceerd, wat betekent dat atomen die vroeger equivalent waren, dat nu niet meer zijn. Substitutie van twee of meer equivalente atomen door hetzelfde element kan dus meer dan één positie-isomeer opleveren.
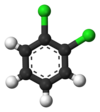
Het klassieke voorbeeld zijn de derivaten van benzeen. De zes hydrogenen zijn alle structureel equivalent, evenals de zes koolwaterstoffen; omdat de structuur niet verandert als de atomen worden gepermuteerd op manieren die overeenkomen met het omdraaien van het molecuul of het roteren ervan met veelvouden van 60 graden. Daarom levert vervanging van een waterstof door chloor slechts één chloorbenzeen op. Maar door die vervanging zijn de atoompermutaties die de waterstof verplaatst hebben niet langer geldig. Er blijft slechts één permutatie over, die overeenkomt met het omdraaien van het molecuul terwijl het chloor gefixeerd blijft. De vijf overblijvende hydrogenen vallen dan in drie verschillende equivalentieklassen: degene tegenover het chloor is een klasse op zichzelf (de para-positie genoemd), de twee die het dichtst bij het chloor liggen vormen een andere klasse (ortho), en de resterende twee vormen de derde klasse (meta). Zo kan een tweede substitutie van waterstof door chloor drie positie-isomeren opleveren: 1,2- of ortho-, 1,3- of meta-, en 1,4- of para-dichloorbenzeen.
 |
 |
 |
| ortho-Dichloorbenzeen | meta-Dichloorbenzeen | para-Dichloorbenzeen |
| 1,2-Dichloorbenzeen | 1,3-Dichloorbenzeen | 1,4-Dichloorbenzeen |
Om dezelfde reden is er maar één fenol (hydroxybenzeen), maar drie benzeendiolen; en één tolueen (methylbenzeen), maar drie toluolen, en drie xylenen.
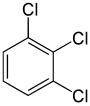
Aan de andere kant kan bij de tweede vervanging (door dezelfde substituent) de symmetrie van het molecuul behouden blijven of zelfs toenemen, en kan dus het aantal equivalentieklassen voor de volgende vervanging behouden blijven of afnemen. Zo vallen de vier overblijvende hydrogenen in meta-dichloorbenzeen nog steeds in drie klassen, terwijl die van ortho- in twee vallen, en die van para- weer allemaal equivalent zijn. Toch leveren sommige van deze 3 + 2 + 1 = 6 substituties uiteindelijk dezelfde structuur op, zodat er slechts drie structureel verschillende trichloorbenzenen zijn: 1,2,3-, 1,2,4-, en 1,3,5-.
 |
 |
 |
| 1,2,3-Trichloorbenzeen | 1,2,4-Trichloorbenzeen | 1,3,5-Trichloorbenzeen |
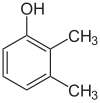
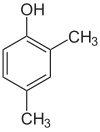
Als de substituenten bij elke stap verschillend zijn, zullen er meestal meer structurele isomeren zijn. Xylenol, dat benzeen is met één hydroxylsubstituent en twee methylsubstituenten, heeft in totaal 6 isomeren:
 |
 |
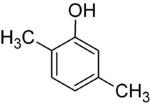 |
| 2,3-Xylenol | 2,4-Xylenol | 2,5-Xylenol |
 |
 |
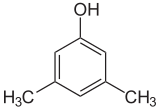 |
| 2,6-Xylenol | 3,4-Xylenol | 3,5-Xylenol |